(9分) 现有FeCl3、AlCl3的混合溶液100mL,逐滴加入NaOH溶液,生成沉淀的物质的量随加入的NaOH的物质的量的关系如图,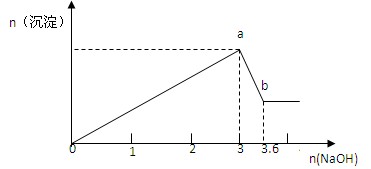
请计算出(1)a处沉淀的总物质的量 mol;
(2)c(FeCl3)= mol/L ; (3)c(AlCl3)= mol/L
为测定某工厂烟道气中SO2的含量,使16.00L烟道气缓慢通过1L水,设SO2完全被吸收,且溶液体积不改变。取出其中20.00mL溶液,加入2—3滴淀粉溶液后,用1.18×10-3mol/L的饱和碘水(密度为1g/cm3)滴定,耗去19.07mL达到终点。(反应为SO2+I2+2H2O→H2SO4+2HI)求
(1)实验条件下碘的溶解度;
(2)该厂烟道气中SO2的含量(mg/L);
(3)为简便计算,在其余操作都不变的情况下,要使滴定时每水泵5mL碘水相当于烟道气中含SO21mg./L,则所配制的碘水的物质的量浓度为多少?
NO2-是一种常见配体,在八面体配离子[MR2(NO2)4]-中,中心离子M含量为21.27%,氮元素的含量为30.33%,只检测到一种N-O键长,请回答下列问题
⑴ 给出自由状态下的NO2-的结构,NO2-在该配合物中配位方式
⑵ 通过计算,给出配离子的化学式和名称
⑶ 画出该配离子的结构
某温度下,测得 氢氧化钠的PH=11水的离子积常数KW是多少?
氢氧化钠的PH=11水的离子积常数KW是多少?
(1)该温度下,水的离子积常数KW是多少?
(2)在此温度下,将pH=a的NaOH溶液VaL与pH=b的硫酸VbL混合。
①若所得混合溶液为中性,且a=12,b=2,则Va : Vb为多少?
②若所得混合溶液为中性,且a+b=12,则Va : Vb为多少?
25℃时,若体积为Va、pH=a的某一元强酸与体积Vb、pH=b的某一元强碱混合,恰好中和,且已知Va<Vb和a=0.5b,请填写下列空白;a值可否等于3(填“可”或“否”)_________,其理由是___________________
a值可否等于5(填“可”或“否”)________,其理由是____________________
a的取值范围是_______________________________________。
25℃时,若体积为Va、pH=a的某一元强酸与体积Vb、pH=b的某一元强碱混合,恰好中和,且已知Va<Vb和a=0.5b,请填写下列空白;a值可否等于3(填“可”或“否”)_________,其理由是___________________
a值可否等于5(填“可”或“否”)________,其理由是____________________
a的取值范围是_______________________________________。