某研究小组在实验室探究氨基甲酸铵(NH2COONH4)分解反应平衡常数。
(1)将一定量纯净的氨基甲酸铵固体置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:
NH2COONH4(s) 2NH3(g)+CO2(g)
2NH3(g)+CO2(g)
实验测得不同温度下的平衡数据列于下表:
| 温度/℃ |
15.0 |
20.0 |
25.0 |
30.0 |
35.0 |
| 平衡总压 强/kPa |
5.7 |
8.3 |
12.0 |
17.1 |
24.0 |
| 平衡气体 总浓度/ mol·L-1 |
2.4× 10-3 |
3.4× 10-3 |
4.8× 10-3 |
6.8× 10-3 |
9.4× 10-3 |
(1)可以判断该分解反应已经达到平衡的是( )
A.2v(NH3)=v(CO2)
B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变
D.密闭容器中氨气的体积分数不变
(2)该分解反应的平衡常数表达式为____________________________,根据表中数据,列式计算25.0 ℃时的分解平衡常数:____________________。(保留两位有效数字)
(3)取一定量的氨基甲酸铵固体放在一个带活塞的密闭真空容器中,在25.0 ℃下达到分解平衡。若在恒温下压缩容器体积,氨基甲酸铵固体的质量________(填“增加”“减少”或“不变”);
(4)氨基甲酸铵分解反应的焓变ΔH________0(填“>”“=”或“<”),熵变ΔS________0 (填“>”“=”或“<”)。此反应在该温度下能自发进行原因是 ________ 效应大于 ___________效应.
(11分) 用化学用语按要求填空:
(1)用系统命名法对下列有机物进行命名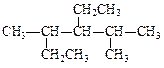 _________________________________
_________________________________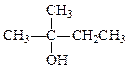 _________________________________
_________________________________
(2)试写出HCHO与足量银氨溶液反应的化学方程式
____________________________________________________________________
(3)TNT的结构简式_________________________________
(4)写出 的结构简式________________________________
的结构简式________________________________
A、B两种固体,都由甲、乙两种元素组成。在A、B中,甲(金属元素)、乙(非金属元素)两种元素的原子个数比分别为1:1和1:2。高温煅烧A、B时,产物都是C(固体)和D(气体)。由D可制得E(酸),E和另一种酸组成的混合酸跟甲苯反应可生成三硝基甲苯。C与E的稀溶液反应得到溶液F,往F溶液中加入NaOH溶液,有红褐色沉淀生成,该沉淀经灼烧后转变成C。往F溶液中加入甲元素的单质得到溶液G。试根据以上信息填写下列空白:
(1)A的化学式是
(2)B煅烧生成C和D的化学方程式是
(3)甲元素的单质与F溶液反应的离子方程式是
(4)往G溶液中加入NaOH溶液发生的现象是,
写出该反应的化学方程式、。
(5)工业上用D制E时,在原料气相同的情况下,测得压强对D平衡转化率的影响见下表:根据表中数据,考虑综合经济效益,你认为该反应应在下列哪中压强下进行最为有利:。
| 0.1MPa |
0.5MPa[ |
1 MPa |
10 MPa |
|
| 400℃ |
99.2% |
99.6%[ |
99.7% |
99.9%[来 |
| 500℃ |
93.5% |
96.9% |
97.8% |
99.3% |
| 600℃ |
73.7% |
85.8% |
89.5% |
96.4% |

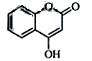
 是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成:
是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成: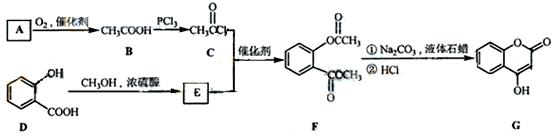


 (1)A与银氨溶液反应有银镜生成,则A的结构简式是。
(1)A与银氨溶液反应有银镜生成,则A的结构简式是。 (2)B→C的反应类型是。
(2)B→C的反应类型是。 (3)E的结构简式是
(3)E的结构简式是 (4)写出F和过量NaOH溶液共热时反应的化学方程式:
(4)写出F和过量NaOH溶液共热时反应的化学方程式:
 (5)下列关于G的说法正确的是
(5)下列关于G的说法正确的是 a.能与溴单质反应 b. 能与金属钠反应
a.能与溴单质反应 b. 能与金属钠反应 c. 1molG最多能和3mol氢气反应 d. 分子式是C9H6O3
c. 1molG最多能和3mol氢气反应 d. 分子式是C9H6O3
按要求写出下列化学方程式:(请注明反应条件)
(1) 甲苯 →TNT
(2) 丙烯 → 聚丙烯
(3)  2-溴丙烷→丙烯
2-溴丙烷→丙烯
有A、B 、C、D 4种短周期元素,它们的原子序数由A到D依次增大。①D的氧化物分子式为DO,在D的氧化物中,氧的质量分数为40%,而且D的原子核中,质子数和中子数相等。②A和B原子有相同的电子层数,A原子的最外层电子数是次外层电子数的2倍。③B的阴离子与C的阳离子和Ne原子的电子层结构相同。在一定条件下0.1 mol单质B2 和0.2 mol H2 恰好完全反应,生成0.2 mol氢化物。④C的单质在点燃条件下与B的单质充分反应,可
、C、D 4种短周期元素,它们的原子序数由A到D依次增大。①D的氧化物分子式为DO,在D的氧化物中,氧的质量分数为40%,而且D的原子核中,质子数和中子数相等。②A和B原子有相同的电子层数,A原子的最外层电子数是次外层电子数的2倍。③B的阴离子与C的阳离子和Ne原子的电子层结构相同。在一定条件下0.1 mol单质B2 和0.2 mol H2 恰好完全反应,生成0.2 mol氢化物。④C的单质在点燃条件下与B的单质充分反应,可 生成浅黄色固体,此生成物又可与A、B化合物反应生成B的单质。
生成浅黄色固体,此生成物又可与A、B化合物反应生成B的单质。
(1)写出下列代号对应的元素符号:D _______。
(2)写出AB2的结构式________,所含化学键的类型_________。
(填字母代号A离子键B极性键C非极性键)
(3)B、C两元素可形成两种不同的化合物,写出它们的电子式:___________、____________。
(4)A元素某氧化物与C元素某氧化物反应生成单质的化学方程式是__________________ ___。
___。