研究物质的微观结构,有助于人们理解物质变化的本质。请回答下列问题:
(1)O、Si、N元素的电负性由大到小的顺序是_______________。
C60和金刚石都是碳的同素异形体,二者比较熔点高的是_______,原因是________________。
(2)利用CO可以合成化工原料COCl2、配合物Fe(CO)5等。
①COCl2分子的结构式为 每个COCl2分子内含有 个δ键, 个π键。其中心原子采取 杂化轨道方式。
每个COCl2分子内含有 个δ键, 个π键。其中心原子采取 杂化轨道方式。
②Fe(CO)5在一定条件下发生分解反应:Fe(CO)5(s)=Fe(s)+5CO(g)反应过程中,断裂的化学键只有配位键,则形成的化学键类型是_______________。
(3)CaTiO3晶体中(晶胞结构如图所示),Ti4+的氧配位数为________;晶体中,若将Ti4+置于立方体的体心,Ca2+置于立方体的顶点,则O2-处于立方体的______; 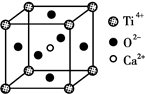
B、D、E为中学化学常见的单质,其中D、E为金属。在一定条件下C、D间能发生反应。各物质转化关系如下图: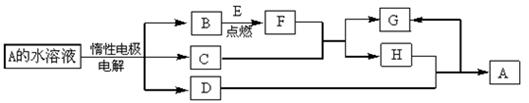
(1)B的同素异形体的名称为:_____________;H的化学式为:_____________。
(2)已知1g E在氧气中燃烧放出的热量为Q kJ,试写出表示E燃烧热的热化学方程式_____________。
(3)用惰性电极电解A 溶液的阳极反应式为:_____________。
(4)检验H和G的混合溶液中含有G的阳离子的试剂可以是:_____________。
a.氯水和KSCN溶液 b.氢氧化钠溶液 c. 酸性KMnO4溶液
(5)用惰性电极电解一定浓度的A溶液,通电一段时间后,向所得溶液中加入8.0g A的氧化物后恰好恢复到电解前的浓度和pH。则电解过程中转移电子的物质的量为_____________mol, 收集到标准状况下的气体体积为_____________。
CO、CH4均为常见的可燃性气体。
(1)等体积的CO和CH4在相同条件下分别完全燃烧,转移的电子数之比是
(2)已知在101kPa时,CO的燃烧热为283kJ/mol。相同条件下,若2 molCH4完全燃烧生成液态水,所放出的热量为1 mol CO完全燃烧放出热量的6.30倍,CH4完全燃烧反应的热化学方程式是。
(3)120℃、101kPa下,a mL由CO、CH4组成的混合气体在b mLO2中完全燃烧后,恢复到原温度和压强。
①若混合气体与O2恰好完全反应,产生bmL CO2,则混合气体中CH4的体积分数为
(保留2位小数)。
②若燃烧后气体体积缩小了a/4mL,则a与b关系的数学表示式是。
短周期的五种元素A、B、C、D、E,原子序数依次增大。A、B、C三种元素原子核外电子层数之和是5。A、B两元素原子最外电子层上电子数之和等于C元素原子最外电子层上的电子数;B元素原子最外电子层上的电子数是它的电子层数的2倍,A和C可以形成化合物CA3;B与D的原子序数之比为3︰4;E原子最外层电子数比次外层电子数少1。请回答:
(1)E在元素周期表的位置为:_▲_
(2)A、B、C、D原子半径从大到小的顺序为:_▲_(填元素符号)
(3)由A、B两种元素组成的分子有多种,其中一种分子含4个原子,且分子为直线型的对称结构,写出其电子式_▲_。
(4)甲由A、B、C、D四种元素组成的无机盐,既可以与盐酸反应又可以与NaOH溶 液反应,其化学式为_▲_。
液反应,其化学式为_▲_。
(5)由A、C、E三种元素组成的化合物C2A6E2是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与NH4Cl类似。写出该化合物第一步水解反应的离子方程式_▲_。
(6)胶态磁流体在医学上有重要的用途,而纳米级Fe3O4是磁流体中的重要粒子,其制备过程简单表示如下:
①将化合物CA3通入等物质的量混合的FeSO4、Fe2(SO4)3溶液中,生成两种碱,写出该过程的总离子方程式_▲_。
②上述反应生成的两种碱继续作用,得到Fe3O4,该反应的化学方程式为_▲_。
(11分) Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl4—SOCl2。电池的总反应可表示为:4Li+2SOCl2 =" 4LiCl" +S +SO2。
Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是LiAlCl4—SOCl2。电池的总反应可表示为:4Li+2SOCl2 =" 4LiCl" +S +SO2。 请回答下列问题:
请回答下列问题: (1)电池的负极材料为,发生的电极反应为;
(1)电池的负极材料为,发生的电极反应为; (2)电池正极发生的电极反应为;
(2)电池正极发生的电极反应为; (3)SOCl2易挥发,实验室中常用NaOH溶液吸收SOCl2,有Na2SO3和NaCl生成。如果把少量水滴到SOCl2中,实
(3)SOCl2易挥发,实验室中常用NaOH溶液吸收SOCl2,有Na2SO3和NaCl生成。如果把少量水滴到SOCl2中,实 验现象是,反应的化学方程式为;
验现象是,反应的化学方程式为; (4)组装该电池必须在无水、无氧的条件下进行,原因是。
(4)组装该电池必须在无水、无氧的条件下进行,原因是。
(4分) (1)KO2能吸收CO2生成K2CO3和O2,故可用作特殊情况下的氧气源,试写出该反应的化学方程式____________________________。
(2)人体内O2-离子对健康有害,使人过早衰老,但在催化剂SOD存在下可发生如下反应,请完成该反应的离子方程式: _O2- +_H2O=__H2O2 + __ O2+ __
_O2- +_H2O=__H2O2 + __ O2+ __