某化学小组采用类似制乙酸乙酯的装置(如图),以环己醇制备环己烯。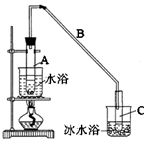
已知:
| |
密度(g/cm3) |
熔点(℃) |
沸点(℃) |
溶解性 |
| 环已醇 |
0.96 |
25 |
161 |
能溶于水 |
| 环已烯 |
0.81 |
-103 |
83 |
难溶于水 |
(1)制备粗品:将12.5 mL环己醇加入试管A中,再加入l mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①A中碎瓷片的作用是_____________,导管B除了导气外还具有的作用是_______ _________。
②试管C置于冰水浴中的目的是 ___________________。
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在_____层(填上或下),分液后用________(填入编号)洗涤。
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3溶液
②再将环己烯按右图装置蒸馏,冷却水从_________(填入编号)口进入。蒸馏时要加入生石灰的目的是____________。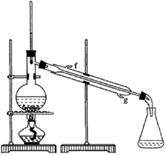
③收集产品时,控制的温度应在_______左右,实验制得的环己烯精品质量低于理论产量,可能的原因是_________________________________________。
a.蒸馏时从70℃开始收集产品
b.环己醇实际用量多了
c.制备粗品时环己醇随产品一起蒸出
(3)以下区分环己烯精品和粗品的方法,合理的是___________。
a、用酸性高锰酸钾溶液 b、用金属钠 c、测定沸点
用18 mol/L H2SO4配制100 mL 1.0mol/L H2SO4,若实验仪器有A.100m L 量筒 B.托盘天平 C.玻璃棒 D.50m L容量瓶 E.10m L量筒 F.胶头滴管 G.50m L烧杯 H.100m L 容量瓶
(Ⅰ)实验时选用的仪器有(填序号)________________________配制过程中,下列情况会使配制结果偏高的是(填序号)_______。
①定容时俯视刻度线观察液面
②容量瓶使用时未干燥
③定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度
(Ⅱ)在容量瓶使用方法中,下列操作不正确的是(填序号)_______________
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再 用待配液润洗
用待配液润洗
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加入蒸馏水到接近刻度线1~2㎝处,再改用胶头滴管加蒸馏水到刻度线
D.配制溶液时,如果试样是液体,用量筒量取试样后直接倒入容量瓶中,缓慢加入蒸馏水到接近刻度线线1~2㎝处,再改用胶头滴管加蒸馏水到刻度线
E.盖好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转摇匀
实验室需要0.1 mol/L NaOH溶液450 mL根据计算用托盘天平称取NaOH的质量为g。在实验中其他操作均正确,若定容时仰视刻度线,则所得溶液浓度0.1 mol/L
(填“大于”、“等于”或“小于”,下同)。若NaOH在溶解后未冷却到室温,便注入容量瓶内并将洗涤液一并转移到容量瓶,并定容,则所得溶液浓度0.1 mol/L。
某溶液中只含有Na2SO4、Na2CO3和NaCl三种溶质。欲证明其中SO42-、CO32-、Cl- 三种阴离子确实存在,我们设计了如下实验,请你认真填写下面的实验报告。
| 实验步骤 |
实验现象 |
结论 |
1、向盛放溶液的试管中加入足量。 |
有气泡产生 |
证明有CO32- |
 2、继续向试管中加入足量溶液 |
有白色沉淀生成 |
证明有。 |
3、过滤,向滤液中加适量的溶液 |
有白色沉淀生成 |
证明有  。 。 |
某同学用托盘天平称量烧杯的质量,天平平衡后的状态如图.由图中可以看出,该同学在操作时的一个错误是______________,烧杯的实际质量为___________g.
(本题8分)如图所示,将甲、乙两个装有不同物质的针筒用导管连接起来 ,将乙针筒内的物质压到甲针筒内,进行下表所列的不伺实验(气体在同温同压下测定)。
,将乙针筒内的物质压到甲针筒内,进行下表所列的不伺实验(气体在同温同压下测定)。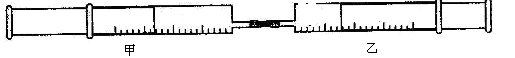
试回答下列问题:
(1)实验1中,沉淀最终变为:色,写出沉淀变色 的化学方程式。
的化学方程式。
(2)实验2中,已知:3Cl2+2NH3=N2+6HCl。甲针筒除活塞有移动, 针筒内有白烟产生外,气体的颜色变化为,最后两个针筒中共剩余气体的体积约为mL。