已知:G、Q、R、T、X、Y、Z都是周期表中前四周期的元素,它们的核电荷数依次增大。G的简单阴离子最外层有2个电子,Q原子最外层电子数是内层电子数的两倍,X元素最外层电子数与最内层电子数相同;T2R的晶体类型是离子晶体,Y原子基态3p原子轨道上有2个未成对电子,其单质晶体类型属于原子晶体;在元素周期表中Z元素位于第10列。
回答下列问题:
⑴Z的核外电子排布式是 。
⑵X以及与X左右相邻的两种元素,其第一电离能由小到大的顺序为 。
⑶QR2分子中,Q原子采取 杂化,写出与QR2互为等电子体的一种分子的化学式: 。
⑷分子式为Q2G6R的物质有两种,其中一种易溶于水,原因是 ;T的氯化物的熔点比Y的氯化物的熔点高,原因是 。
⑸据报道,由Q、X、Z三种元素形成的一种晶体具有超导性,其晶体结构如图所示。晶体中距每个X原子周围距离最近的Q原子有 个。
高炉炼铁中发生的基本反应之一如下:
FeO(s)+ CO (g)  Fe(s)+ CO2(g)△H>0
Fe(s)+ CO2(g)△H>0
(1)此反应的平衡常数表达式为:K=
(2)温度升高,达到新的平衡后,高炉内CO2与CO的体积比(填“增大”、 “减小”或“不变”)。
(3)已知1100℃时,K= 0.263。某时刻测得高炉中c(CO2)=" 0.025" mol·L-1,c(CO)=" 0.1" mol·L-1,在这种情况下,该反应(填“是”或“不是”)处于化学平衡状态。
如果“不是”,此时化学反应向方向进行(填“正反应”或“逆反应”)。如果“是”,此空不填
日常生活中,可用明矾[KAl(SO4)2·12H2O]作为净水剂,这是因为:明矾溶于水发生水解反应,生成氢氧化铝胶体,氢氧化铝胶体可以吸附杂质。写出水解反应的离子方程式为:
pH = 2与pH = 5的两强酸溶液各10 mL,混合后溶液的pH为。
纯水在20 ℃的pH(填“大于”或“小于”)80 ℃时的pH。
可逆反应: 根据图回答:
根据图回答: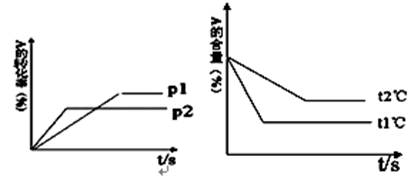
(1)压强 P1比P2(填“大”或“小”);
(2)(a +b)比(c +d)(填“大”或“小”);
(3)温度t1℃比t2℃(填“高”或“低”);
(4)正反应为反应(填“吸热”或“放热”);