25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应:
Sn(s)+Pb2+(aq) Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示。下列判断正确的是( )
Sn2+(aq)+Pb(s),体系中c(Pb2+)和c(Sn2+)变化关系如图所示。下列判断正确的是( )
| A.往平衡体系中加入金属铅后,c(Pb2+)增大 |
| B.往平衡体系中加入少量Sn(NO3)2固体后,c(Pb2+)变小 |
| C.升高温度,平衡体系中c(Pb2+)增大,说明该反应△H>0 |
| D.25℃时,该反应的平衡常数K=2.2 |
下列物质按纯净物、混合物、电解质、非电解质的顺序组合的一组为
| A.纯盐酸、空气、硫酸、干冰 |
| B.蒸馏水、氨水、碳酸氢钠、二氧化硫 |
| C.胆矾、盐酸、铁、碳酸钙 |
| D.生石灰、漂白粉、氯化铜、碳酸钠 |
下列说法正确的是
| A.我国自主研发的“龙芯1号”CPU芯片与光导纤维是同种材料 |
| B.需要通过化学反应才能从海水中获得食盐和淡水 |
| C.水晶项链和餐桌上的瓷盘都是硅酸盐制品 |
| D.工业制粗硅涉及氧化还原反应 |
下列对化学知识概括合理的是
| A.酸性氧化物都是非金属氧化物 |
| B.一种元素可能有多种氧化物,但同种化合价只对应一种氧化物 |
| C.丁达尔效应可用于区别溶液与胶体,云、雾均能产生丁达尔效应 |
| D.熔融状态能导电的物质一定是离子化合物 |
实验是化学研究的基础。下列关于各实验装置的叙述正确的是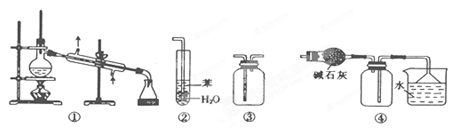
| A.装置③可用于收集H2、CO2、Cl2、NH3等气体 |
| B.装置②可用于吸收NH3或HCl气体,并防止倒吸 |
| C.装置①常用于分离互不相溶的液体混合物 |
| D.装置④可用于干燥、收集氯化氢,并吸收多余的氯化氢 |
有关下列图象的说法正确的是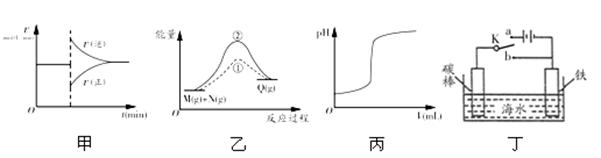
| A.图甲中的曲线可以表示某化学平衡体系改变温度后反应速率随时间的变化 |
| B.图乙中①、②曲线分别表示反应M(g)+N(g)→Q(g),ΔH>0使用和未使用催化剂时,反应过程中的能量变化 |
| C.图丙中的曲线可表示向一定量的氢氧化钠溶液中滴加一定浓度盐酸时的pH变化 |
| D.图丁中开关K置于a或b处均可减缓铁的腐蚀 |