决定物质性质的重要因素是物质结构。请回答下列问题。
(1)已知A和B为第三周期元素,其原子的第一至第四电离能如下表所示:
| 电离能/kJ·mol-1 |
I1 |
I2 |
I3 |
I4 |
| A |
578 |
1817 |
2745 |
11578 |
| B |
738 |
1451 |
7733 |
10540 |
A通常显________价,A的电负性_____B的电负性(填“>”、“<”或“=”)。
(2)已知:波长为300nm的紫外光的光子所具有的能量约为399 kJ/mol。根据下表有关蛋白质分子中重要化学键的信息,说明人体长时间照射紫外光后皮肤易受伤害的原因:______________________
| 共价键 |
C-C |
C-N |
C-S |
| 键能/ kJ·mol-1 |
347 |
305 |
259 |
(3)研究物质磁性表明:金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是__________________。
、
、
、
、
为短周期元素,非金属元素
最外层电子数与其周期数相同,
的最外层电子数是其所在周期数的2倍。
在
中充分燃烧能生成其最高价化合物
。
与
具有相同的电子数。
在
中燃烧,产物溶于水得到一种强酸。回答下列问题:
(1)
在周期表中的位置是,写出一种工业制备单质F的离子方程式。
(2)
、
、
组成的一种盐中,
的质量分数为43%,其俗名为,其水溶液与
单质反应的化学方程式为;在产物中加入少量
,反应后加人
并振荡,有 机层显色。
(3)由这些元素组成的物质,其组成和结构信息如下表:
| 物质 |
组成和结构信息 |
| 含有
的二元离子化合物 |
|
| 含有非极性共价键的二元离子化合物,且原子数之比为1:1 |
|
| 化学组成为 | |
| 只存在一种类型作用力且可导电的单质晶体 |
的化学式为;
的化学式为;
的电子式为;
的晶体类型是。
(4)由
和
、
元素组成的两种二元化合物形成一类新能源物质。一种化合物分子通过键构成具有空腔的固体;另一种化合物(沼气的主要成分)分子进入该空腔,其分子的空间结构为。
[物质结构与性质]
含有
的
悬浊液可用于检验醛基,也可用于和葡萄糖反应制备纳米
。
(1)
+基态核外电子排布式为
(2)与
-互为等电子体的一种分子为(填化学式)。
(3)醛基中碳原子的轨道杂化类型是;
乙醛分子中含有
的键的数目为。
(4)含有
的
悬浊液与乙醛反应的化学方程式为。
(5)
在稀硫酸中生成
和
。铜晶胞结构如图所示,铜晶体中每个铜原子周围距离最近的铜原子数目为。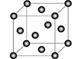
硫化氢的转化是资源利用和环境保护的重要研究课题。由硫化氢获得硫单质有多种方法。
(1)将烧碱吸收
后的溶液加入到如题20图-1所示的电解池的阳极区进行电解。电解过程中阳极区发生如下反应:
①写出电解时阴极的电极反应式:。
②电解后阳极区的溶液用稀硫酸酸化得到硫单质,其离子方程式可写成。
(2)将
和空气的混合气体通入
、
、
的混合溶液中反应回收
,其物质转化如题20图-2所示。
①在图示的转化中,化合价不变的元素是。
②反应中当有1
转化为硫单质时,保持溶液中
的物质的量不变,需要消耗
的物质的量为。
③在温度一定和不补加溶液的条件下,缓慢通入混合气体,并充分搅拌。欲使生成的硫单质中不含
,可采取的措施有。
(3)
在高温下分解生成硫蒸气和
。若反应在不同温度下达到平衡时,混合气体中各组分的体积分数如题20图-3所示,
在高温下分解反应的化学方程式为。


非诺洛芬是一种治疗类风湿性关节炎的药物,可通过以下方法合成:
请回答下列问题:
(1)非诺洛芬中的含氧官能团为和(填名称)。
(2)反应①中加入的试剂
的分子式为
,
的结构简式为(3)在上述五步反应中,属于取代反应的是(填序号)。
(4)
的一种同分异构体满足下列条件:
Ⅰ.能发生银镜反应,其水解产物之一能与
溶液发生显色反应。
Ⅱ.分子中有6种不同化学环境的氢,且分子中含有两个苯环。
写出该同分异构体的结构简式:
(5)根据已有知识并结合相关信息,写出以 为原料制备
为原料制备 的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
烟气脱硫能有效减少二氧化硫的排放。实验室用粉煤灰(主要含 、 等)制备碱式硫酸铝溶液,并用于烟气脱硫研究。

(1)酸浸时反应的化学方程式为;滤渣Ⅰ的主要成分为(填化学式)。
(2)加
调节溶液的
至3.6,其目的是中和溶液中的酸,并使
转化为
。滤渣Ⅱ的主要成分为(填化学式);若溶液的
偏高,将会导致溶液中铝元素的含量降低,其原因是(用离子方程式表示)。
(3)上述流程中经完全热分解放出的 量总是小于吸收的 量,其主要原因是;与吸收 前的溶液相比,热分解后循环利用的溶液的 将(填"增大"、"减小"或"不变")。