向下列各物质的水溶液中滴加稀H2SO4或MgCl2溶液时,均有白色沉淀生成的是
| A.Ba(OH)2 | B.BaCl2 | C.Na2CO3 | D.KOH |
对于锌、铜和稀硫酸组成的原电池(如图),下列有关说法不正确的是( )
| A.Zn是负极 | B.Cu是正极 |
| C.负极上发生氧化反应 | D.正极上发生氧化反应 |
把a、b、c、d四块金属片浸入稀硫酸中,用导线两两相连组成原电池。若a、b相连时,a为负极;c、d相连时,电流由d到c;a、c相连时c极上产生大量气泡。b、d相连时,b上有大量气泡产生,则四种金属的活动性顺序由强到弱的顺序为( )
| A.a>b>c>d | B.a>c>d>b | C.c>a>b>d | D.b>d>c>a |
将锌片和铜片按图示方式插入柠檬中,电流计指针发生偏转。下列针对该装置的说法正确的是( )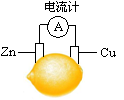
| A.将电能转化为化学能 |
| B.电子由铜片流出 |
| C.锌片是负极. |
| D.铜片逐渐被腐蚀 |
下列为原电池装置的是( )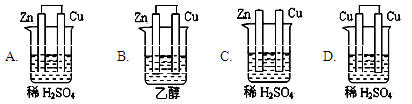
下图各装置中,不能构成原电池的是(烧杯中所盛液体都是稀硫酸)( )