下列各组离子能大量共存的是( )
| A.H+、K+、Cl-、OH- | B.Na+、Cu2+、NO3-、SO42- |
| C.K+、Ca2+、NO3-、CO32- | D.Na+、Ag+、NO3-、Cl- |
下列说法正确的是
| A.用重结晶法除去NaCl晶体中混有的少量KNO3时,将样品配成饱和溶液并放入蒸发皿中蒸发,当只剩下少量溶液时停止加热,利用余热蒸干 |
| B.同温同压下,相同体积的0.1 mol▪L—1一元酸A和1 mol▪L—1一元酸B分别与总表面积相同的一定质量的锌粉反应时,发现前者放出H2的速率大,可以证明A的酸性大于B |
| C.准确度体现了测定结果的再现性,用偏差表示,偏差越小,说明测定的结果的准确度越高 |
| D.碱石灰(NaOH和CaO的混合物)是一种实验室中常用的干燥剂,能用吸收水蒸气和二氧化碳,吸收过程中起主要作用的物质是CaO |
向CuSO4溶液中逐滴加入过量KI溶液,观察到产生白色沉淀,溶液变为棕色。再向反应后的混合物中不断通入SO2气体,溶液逐渐变成无色。则下列分析中正确的是
| A.白色沉淀是CuI2,棕色溶液含有I2 |
| B.滴加KI溶液时,转移1 mol电子时生成1 mol白色沉淀 |
| C.通入SO2时,SO2与I2反应,I2作还原剂 |
| D.上述实验条件下,物质的氧化性:Cu2+> SO2> I2 |
一定条件下,电解较稀的硫酸,其还原产物为双氧水,该原理可用于制取双氧水,其电解的化学方程式为:3H2O+3O2===O3+3H2O2。下列有关说法正确的是
| A.电解池的阳极生成双氧水,阴极生成臭氧 |
| B.电解池中硫酸溶液的pH保持不变 |
| C.产生臭氧的电极反应式为3H2O-6e-===O3+6H+ |
| D.产生双氧水的电极反应式为2H2O-2e-===H2O2+2H+ |
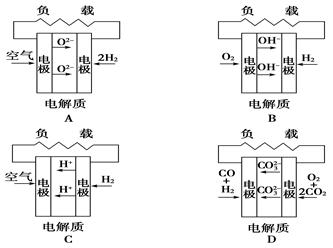
有四种燃料电池,
| A.固体氧化物燃料电池, | B.碱性氢氧化物燃料电池, | C.质子交换膜燃料电池, | D.熔融盐燃料电池,下面是工作原理示意图,其中正极反应生成水的是 |
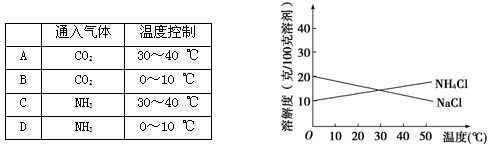
联合制碱法中关键的一步是把NH4Cl从几乎饱和的NaHCO3溶液中分离出来,为此根据NaCl和NH4Cl溶解度的差异,向混合溶液中通入某种气体,同时加入磨细的食盐,可析出不夹带NaHCO3的NH4Cl。NaCl和NH4Cl共同存在时的溶解度曲线如下图所示,则正确的操作是