工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大损害,必须进行处理。常用的处理方法有两种。其中一种方法是还原沉淀法
该法的工艺流程为:CrO42- Cr2O72-
Cr2O72-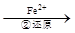 Cr3+
Cr3+ Cr(OH)3↓
Cr(OH)3↓
其中第①步存在平衡:2CrO42-(黄色)+2H+ Cr2O72-(橙色)+H2O
Cr2O72-(橙色)+H2O
(1)若该平衡处在强酸性环境,则溶液显________色。
(2)能说明第①步反应达平衡状态的是 。
A. Cr2O72-和CrO42-的浓度相同 B. 2v(Cr2O72-)=v(CrO42-) C.溶液的颜色不变
(3)第②步中,还原1 mol Cr2O72-离子,需要 mol的FeSO4·7H2O。
写出第②步中反应的离子方程式____________________________________。
(4)第③步生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:
Cr(OH)3(s) Cr3+(aq)+3OH―(aq)
Cr3+(aq)+3OH―(aq)
常温下,Cr(OH)3的溶度积Ksp=c(Cr3+)·c3(OH―)=10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至 。
(Ⅰ)糖尿病是由于体内胰岛素紊乱导致的代谢紊乱综合症,以高血糖为主要标志。长期摄人高热量食品和缺少运动都易导致糖尿病。
(1)血糖是指血液中的葡萄糖(C6H12O6)。下列说法正确的是(填字母序号)。
A.葡萄糖属于碳水化合物,分子可表示为C6(H2O)6,则每个葡萄糖分子中含6个H2O
B.糖尿病人尿糖也高,可用新制的氢氧化铜悬浊液来检测病人尿液中的葡萄糖
C.葡萄糖可用于制镜工业
D.淀粉水解的最终产物是葡萄糖
(2)糖尿病人不可饮酒,酒精在肝脏内可被转化成有机物M。M的实验结果如下:
①通过样品的质谱测得M的相对分子质量为60。
②核磁共振氢原子光谱能对有机物分子中同性氢原子给出相同的峰值(信号),根据峰值(信号)可以确定分子中氢原子的种类和数目。例如:乙醇(CH3CH2OH)有三种氢原子(图1)。经测定,有机物M的按磁共振氢谱示意图如下图2。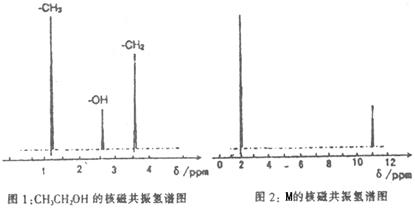
③将M溶于水,滴入石蕊试液,发现溶液变红。试推导写出M的结构简式为。
(Ⅱ)已知物质A显酸性,F为七原子组成的环状结构,请根据以下框图回答问题: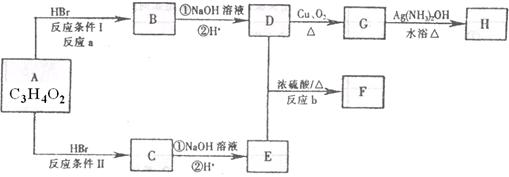
(1) A、H的结构简式为、。
(2)a、b的反应类型分别为、。
(3)D和E生成F的化学方程式。
(4)写出C的同分异构体中属于酯类物质的结构简式、(任写2种)。
根据下列框图回答问题:
已知白色固体N中阴、阳离子具有相同的核外电子层结构。
(1)写出M中存在的离子:
(2)请写出M与N反应的离子方程式:。
(3)写出A在空气中锻烧的化学方程式:。
(4)某同学取H的溶液,通入气体B,所得溶液中仍只有一种阴离子。请写出上
述变化过程中的离子方程式 。
下表是元素周期表的一部分.
(1)表中元素⑩的氢化物的化学式为,此氢化物的还原性比元素⑨的氢化物的还原性(填强或弱)
(2)某元素原子的核外电子层中L层电子数比K层电子数多3,则该元素的元素符号是,其单质的电子式为.
(3)已知某些不同族元素的性质也有一定的相似性,如元素③与元素⑧的氢氧化物有相似的性质。写出元素③的氢氧化物与NaOH溶液反应的化学方程式:
;
又如表中与元素⑦的性质相似的不同族元素是(填元素符号)
(4)元素⑤的氢化物是最重要的氮肥,是产量最大的化工产品之一。课本里介绍的合成氨技术叫哈伯法,是德国人哈伯在1905年发明的,其合成原理为:N2(g)+3H2(g)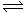 2NH3(g) △H= -92.4kJ/mol,他因此获得了1918年诺贝尔化学奖。试回答下列问题:
2NH3(g) △H= -92.4kJ/mol,他因此获得了1918年诺贝尔化学奖。试回答下列问题:
①合成氨工业中采取的下列措施可用勒夏特列原理解释的是(填序号)
| A.采用较高压强(20Mpa~50Mpa) |
| B.采用500℃的高温 |
| C.用铁触媒作催化剂 |
| D.将生成的氨液化并及时从体系中分离出来,N2和H2循环到合成塔中并补充N2和H2 |
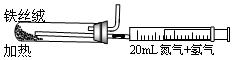
②上图是实验室模拟工业法合成氨的简易装置。简述检验有氨气生成的方法。
③在298K时,将10 mol N2和30 mol H2放入合成塔中,为何放出的热量小于924kJ?
。
④1998年希腊亚里斯多德大学的Marmellos和Stoukides发明一种合成氨的新方法。在常压下,将H2与用He稀释的N2分别通入一加热到570℃的,以锶-铈-钇-钙钛矿多孔陶瓷(SCY)为固体电解质的电解池中转化为氨气(SCY陶瓷能传递H+),H2转化率达到78%。其实验装置如图所示。阴极的电极反应式。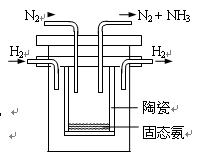
北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6)。
(1)丙烷脱氢可得丙烯。
已知:C3H8(g) ="===" CH4(g)+HC≡CH(g)+H2(g) △H1= +156.6 kJ·mol-1
CH3CH=CH2(g) ="===" CH4(g)+HC≡CH(g) △H 2= +32.4 kJ·mol-1
则相同条件下,反应C3H8(g) ="==" CH3CH=CH2(g)+H2(g)的△H =kJ·mol-1。
(2)以丙烷为燃料制作新型燃料电池,其电解质溶液是氢氧化钾溶液。电池正极反应方程式为:;负极反应方程式:。
(3)碳氢化合物完全燃烧生成CO2和H2O。常温常压下,空气中的CO2溶于水,得到c(H2CO3)=1.5×10-5 mol·L-1的溶液,测得该溶液的pH=5.60。若忽略水的电离及H2CO3的第二级电离,则H2CO3 HCO3-+H+的平衡常数K1=。(已知
HCO3-+H+的平衡常数K1=。(已知
10-5.60=2.5×10-6)
(4)常温下,0.1 mol·L-1 NaHCO3溶液的pH大于8,则溶液中c(H2CO3)c(CO32-)(填“>”、“=”或“<”),原因是(用离子方程式和必要的文字说明)。
(14分)氯化铁是常见的水处理剂,无水FeCl3的熔点为555K、沸点为588K。工业上制备无水FeCl3的一种工艺如图所示。
(1)取0.5mL三氯化铁溶液滴入50mL沸水中,再煮沸片刻得红褐色透明液体,该过程可用离子方程式表示为____________。
(2)下表是六水合氯化铁在水中的溶解度。
| 温度/℃ |
0 |
10 |
20 |
30 |
50 |
80 |
100 |
| 溶解度 /(g/100g H2O) |
74.4 |
81.9 |
91.8 |
106.8 |
315.1 |
525.8 |
535.7 |
从FeCl3溶液中获得FeCl3·6H2O的方法是_______________。
(3)捕集器中温度超过673K,存在相对分子质量为325的物质,该物质的分子式为:______
(4)吸收剂X是________;吸收塔中吸收剂X的作用是________。
(5)FeCl3的质量分数通常可用碘量法测定:称取m g无水氯化铁样品,溶于稀盐酸,再转移到100mL容量瓶,用蒸馏水定容;取出10.00 mL,加入稍过量的KI溶液,充分反应后,用淀粉作指示剂并用c mol/L Na2S2O3溶液滴定(I2+2S2O32— = 2I— + S4O62—),共用去V mL.则样品中氯化铁的质量分数为____________。