实验是学习化学的重要手段,通过实验可以培养实践能力和创新精神。
(一)实验室制取气体是初中一类重要的实验,结合下列仪器或装置图回答有关问题: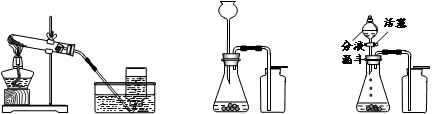
装置I 装置Ⅱ 装置Ⅲ
(1)装置I是用高锰酸钾制氧气,反应的化学方程式为_________________________,表明氧气已经收满的实验现象是 。
(2)某同学用装置Ⅱ制取并收集二氧化碳,用燃着的木条放在集气瓶口验满,始终未发现火焰熄灭,原因是______________________________________________。
(3)用装置Ⅲ进行二氧化锰和双氧水制取氧气的实验时,若反应速率过快,可以采取的处理方法是 。
(4)我们已经学过实验室制取O2、CO2、H2三种气体的反应原理及制取、收集方法。请你归纳出制取这三种气体时反应的共同点_______(填选项序号)。
| A.需要加热 | B.需使用催化剂 |
| C.没有气体参加反应 | D.生成的气体只有一种 |
(二)选用下列装置测定水的元素组成,请回答问题: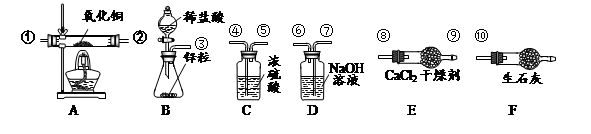
(5)为准确测定水的组成并防止杂质、空气等干扰,导管口的正确连接顺序为:
③→___→____→____→____→①→②→⑧→⑨→⑩。
(6)若测得A装置中样品在实验后减少了6.4克,E装置质量增加了7.2克,F装置增加了0.1克,据此可求出水中H、O元素质量比为(只写计算式)____________。
(7)实验结束后,若A处仍有黑色固体,这对实验结果的影响是________________(填“氧的质量偏大”、“氢的质量偏大”、“无影响”)。
某同学为了研究炼铁的原理并测定生成铁的质量,用一氧化碳与氧化铁反应,按下图进行实验。
(1)首先,该同学称量氧化铁的质量,然后进行实验,他先打开K1,关闭K2,通入一氧化碳,其目的是排尽玻璃管内的空气,防止加热时因一氧化碳不纯而引起爆炸,然后关闭K1,打开K2,加热,反应一段时间后,冷却,再次称量固体的质量,发现固体质量减少了12克,则生成铁的质量为_____,玻璃管中发生反应的化学方程式为_________________。
(2)装置B中反应的化学方程式是________________________________。
(3)装置C的两个作用是________________________________________________,
(4)实验结束后,烧杯内的溶液中含有的溶质是_________________(写化学式)。
现有HCl、NaCl、NaOH、Na2CO3等溶液。若进行下列实验,请判断可能的溶液组合。
(1)两两组合进行实验:
① 组合后无明显现象,但发生反应的组合是____________;
写出该反应的化学方程式为______________________。
② 组合后有明显现象,该现象是__________________。
反应的化学方程式为___________________________________。
(2)任意组合进行实验:
若将氢氧化钙溶液逐滴滴入组合溶液中,产生的沉淀与加入的氢氧化钙有如图所示的关系,则溶液的组合可能是。
已知一种固体化合物由氢、氧、碳、铜四种元素组成,向盛有该化合物的试管中加入稀盐酸时,固体逐渐溶解,有大量气泡产生,得到蓝绿色的氯化铜溶液。
(1)探究产生的气体是什么。
猜想:①可能是氢气;②;③……
实验:请针对你②和③猜想中的一种,设计实验方案,验证你的猜想。
(2)从蓝绿色溶液中提取金属铜。有关实验方案如下:
①操作Ⅰ的名称为;加入过量A的目的是;有关反应的化学方程式为。
②操作II中加入足量B的目的是;确定此目的已经达到的依据是。
根据下表内容进行活动与探究,请你参与并回答问题:
| 实验 名称 |
(1)空气中氧气含量的测定 |
| 实验 设计 |
 (燃烧匙中的药品为红磷) (燃烧匙中的药品为红磷) |
| 问题 与结论 |
①该实验应用的化学方程式为:; ②实验中应该观察到的现象是:。 |
| 实验 名称 |
(2)一氧化碳还原氧化铁 |
| 实验 设计 |
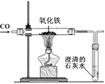 |
| 问题 与结 论 |
①写出氧化铁被还原成铁的反应化学方程式; ②从环保角度分析,该装置有明显的缺陷,你认为是; ③用该图所示装置进行实验时,石灰水所起的作用是。 |
探究实验(共8分)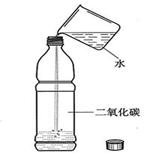

二氧化碳的溶解性实验氢氧化钠溶解于水
A B
(1)探究物质性质
上述A、B两个实验都是通过___ ____的变化来间接感知。B实验中___ ____(填a或b)处的水位升高的。
(2)探究可燃物燃烧条件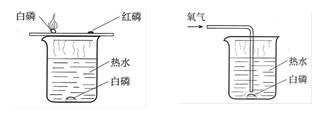
探究燃烧的条件
实验中探究可燃物的燃烧条件,它是通过控制可燃物是否与氧气接触和控制___ ____来探究可燃物燃烧的条件。能证明燃烧必须与氧气接触的实验现象是_____ _____;采用了___ ____的实验手段
(3)物质性质的应用:
| 实验序号 |
实验目的 |
实验方案 |
实验现象 |
结论 |
实验1 |
___ ____ |
 |
___ ____ |
草木灰的主要成分是碳酸钾 |