A、B、C、D、E、F、G七种物质间存在如图所示转化关系,其中A、B、D、G含有同种元素。
已知
(Ⅰ)A为金属单质; B为红褐色固体;E为密度最小的气体;G为浅绿色溶液。
(Ⅱ)D为黄色溶液,能与硝酸银溶液反应生成不溶于稀硝酸的白色沉淀。
(Ⅲ)D能将某种氧化物氧化为F,F是含有三种元素的化合物。
请回答下列问题:
(1)上述反应中属于置换反应的是 (填序号)。
(2)G生成B的过程中所出现的现象 ;
反应③的离子方程式 。
(3)D的水溶液显酸性,请用离子方程式解释原因 。
(4)实验室制取C的化学方程式为 ;
对气体C进行如下实验。已知整个反应过程中,每消耗0.1mol KI,转移的电子数约为3.612×1023 个。请按照要求填空:
| 实验步骤 |
实验现象 |
用化学用语解释 |
| 将少量气体通入淀粉KI溶液 |
溶液最初变成 色 |
(用离子方程式表示) |
| 继续通入气体 |
溶液逐渐变成无色 |
(用化学方程式表示) |
火力发电厂释放出大量的氮氧化物(NOx).二氧化硫和二氧化碳等气体会造成环境污染。对燃煤废气进行脱硝.脱碳和脱硫等处理,可实现绿色环保、节能减排、废物利用等目的。
(1)脱硝。利用甲烷催化还原NOx:
CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g);ΔH1=-574kJ·mol-1
CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g);ΔH2=-1160kJ·mol-1
甲烷直接将NO2还原为N2的热化学方程式为:。
2)脱碳。将CO2转化为甲醇的热化学方程式为:
CO2(g)+3H2(g) CH3OH(g)+H2O(g);ΔH3
CH3OH(g)+H2O(g);ΔH3
① 取五份等体积CO2和H2的混合气体(物质的量之比均为1∶3,分别加入温度不同、容积相同的恒容密闭容器中,发生上述 反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH)与反应温度T的关系曲线如图所示,根据图示 (填写具体的线段)走向,则上述CO2转化为甲醇的反应的ΔH3 0(填“>”.“<”或“=”)。
反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH)与反应温度T的关系曲线如图所示,根据图示 (填写具体的线段)走向,则上述CO2转化为甲醇的反应的ΔH3 0(填“>”.“<”或“=”)。
② 在一恒温恒容密闭容器中充入1mol CO2和3mol H2,进行上述反应。测得CO2和CH3OH(g)的浓度随时间变化如下图所示。下列说法正确的是 (填字母代号)。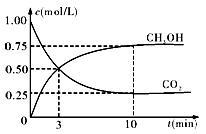
A.第10min后,向该容器中再充入1mol CO2和3mol H2,则再次达到平衡时c(CH3OH) > 1.5 mol·L-1且化学平衡常数K值增大。 mol·L-1且化学平衡常数K值增大。 |
| B.0~10min内,氢气的平均反应速率为0.075mol•(L·min)-1 |
| C.达到平衡时,氢气的转化率为75 % |
| D.第10min后,升高温度将使n(CH3OH)/n(CO2)减小 |
(3)脱硫。燃煤废气经脱碳处理后,用空气氧化,并用氨气吸收生成硫酸铵和硝酸铵的混合物作为副产品化肥。设烟气中的SO2、NO2的物质的量之比为1∶1,则该反应的化学方程式为: 。
(4)硫酸铵和硝酸铵的水溶液的pH<7,其原因可用一个离子方程式表示为: ;在一定物质的量浓度的硝酸铵溶液中滴加适量的NaOH溶液,使溶液的pH=7,则溶液中存在着离子浓度关系为:c(Na+)+c(H+) c(NO)+c(OH-)(填写“>”“=”或“<”)。
茶是我国人民喜爱的饮品。某校化学兴趣小组的同学设计以下实验来定性检验茶叶中含有Ca、A1、Fe三种元素。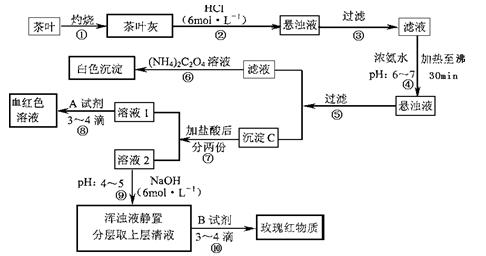
【资料查询】: 草酸铵[(NH4)2C2O4]属于弱电解质。草酸钙(CaC2O4)难溶于水。Ca2+、
草酸铵[(NH4)2C2O4]属于弱电解质。草酸钙(CaC2O4)难溶于水。Ca2+、
A13+、Fe3+完全沉淀的pH:Ca(OH)2:pH≥13;A1(OH)3:pH≥5.5;Fe(OH)3:pH≥4.1。
试根据上述过程及信息填空:
(1)步骤②加盐酸的作用是。
(2)步骤③操作中用到的玻璃仪器有。
(3)写出步骤⑥中检验Ca2+存在的离子方程式。
(4)写出沉淀C所含主要物质的化学式。
(5)写出步骤⑧中选用A试剂的化学式 。
。
(6)步骤⑨的作用是,
猜测步骤⑩的目的是。
第三代混合动力车,可以用电动机、内燃机或二者结合作为动力。汽车在刹车或下坡时,
电池处于充电状态。混合动力车目前一般使用镍氢电池,该电池中镍的化合物为正极,储氢金属(以M表示)为负极,碱液(主要为KOH)为电解质溶液。下图是镍氢电池充放电原理的示意,其总反应式为: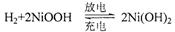 ,下列说法中正确的是
,下列说法中正确的是
| A.混合动力车上坡或加速时,溶液中的OH-向乙电极移动 |
| B.混合动力车刹车或下坡时,乙电极周围溶液的pH增大 |
| C.混合动力车上坡或加速时,乙电极电极反应式为NiOOH+H2O+e-=Ni(OH)2+OH- |
| D.混合动力车刹车或下坡时,甲电极电极反应式为H2+2OH-+2e- =2H2O |
根据下列化学实验示意图及表中实验现象,能得出正确结论的是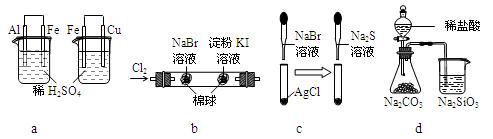
| 选项 |
实验 |
实验现象 |
结论 |
| A |
a |
左烧杯中铁表面有气泡,右烧杯中铜表面有气泡 |
活动性:Al>Fe>Cu |
| B |
b |
左边棉花变为橙色,右边棉花变为蓝色 |
氧化性:Cl2>Br2>I2 |
| C |
c |
白色固体先变为淡黄色,后变为黑色 |
溶解性:AgCl < AgBr< Ag2S |
| D |
d |
锥形瓶中有气体产生,烧杯中液体变浑浊 |
非金属性:Cl>C>Si |
有X、Y、Z、W、M五种短周期元素,其中X、 Y、Z、W同周期, Z、M同主族; X+与M2-具有相同的电子层结构;离子半径:Z2-
>W-;Y的单质晶体熔点高、硬度大,是一种重要的半导体材料。下列说法正确的是
| A.X、M两种元素只能形成X2M型化合物 |
| B.Y、Z两元素的气态氢化物中,Y的气态氢化物更稳定 |
| C.Z、W两元素的最高价氧化物对应水化物的酸性:Z > W |
| D.W、M两元素的某些单质或化合物可作为自来水消毒剂 |