将海水淡化和与浓海水资源化结合起来是综合利用海水的重要途径之一。一般是先将海水淡化获得淡水,再从剩余的浓海水中通过一系列工艺提取其他产品。回答下列问题:
(1)下列改进和优化海水综合利用工艺的设想和做法可行的是 (填序号)。
①用混凝法获取淡水 ②提高部分产品的质量
③优化提取产品的品种 ④改进钾,溴,镁的提取工艺
(2)采用“空气吹出法”从浓海水中吹出Br2,并用纯碱吸收。碱吸收溴的主要反应是:Br2+Na2CO3+H2O  NaBr+NaBrO3+6NaHCO3,吸收1mol Br2时转移的电子为 mol。
NaBr+NaBrO3+6NaHCO3,吸收1mol Br2时转移的电子为 mol。
(3)海水提镁的一段工艺流程如下图:
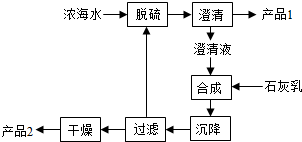
浓海水的主要成分如下:
| 离子 |
Na+ |
Mg2+ |
Cl- |
SO42- |
| 浓度/(g·L-1) |
63.7 |
28.8 |
144.6 |
46.4 |
该工艺过程中,脱硫阶段主要反应的离子方程式为 ,产品2的化学式为 ,1L浓海水最多可得到产品2的质量为 g。
(4)采用石墨阳极.不锈钢阴极电解熔融的氯化镁,发生反应的化学方程式为 ;电解时,若有少量水存在会造成产品镁的消耗,写出有关反应的化学方程式 。
(8分)请回答下列各问:
(1)酸雨的pH范围是,在空气质量报告的各项指标中有可吸入颗粒物,还有。
(2)石灰法是目前应用最广泛的工业废气脱硫方法,过程如下:通过煅烧石灰石得到生石灰,以生石灰为脱硫剂在吸收塔中与废气中的SO2反应而将硫固定,写出反应的化学方程式。
(3)硝酸铜是制备Cu-Zn-Al系催化剂的重要原料,工业上用洗净的废铜屑作原料来制备硝酸铜。下列制备方法符合“绿色化学”思想的是(填序号)。
① Cu + HNO3(浓)→ Cu(NO3)2
② Cu + HNO3(稀)→ Cu(NO3)2
③ Cu  CuO
CuO Cu(NO3)2
Cu(NO3)2
(4)在100mL 18mol·L-1的浓硫酸中加入过量的铜片,加热使之充分反应,产生的气体在标准状况下的体积可能是。
| A.40.32L | B.30.24L | C.20.16L | D.13.44L |
(5)某同学向浸泡铜片的稀盐酸中加入H2O2后,铜片溶解,并且该反应的产物只有氯化铜和水。该反应的化学方程式为。
(12分)在一定温度下将 2 mol A和2 mol B两种气体混合于2 L密闭容器中,发生如下反应:3A(g)+B(g)
2 mol A和2 mol B两种气体混合于2 L密闭容器中,发生如下反应:3A(g)+B(g) 2C(g)+2D(g),2分钟末反应达到平衡状态,生
2C(g)+2D(g),2分钟末反应达到平衡状态,生 成了0.8 mol D,请填写下面空白。
成了0.8 mol D,请填写下面空白。
(1) B的平衡浓度为________。
(2) A的转化率为________。
(3) 用D表示的平均反应速率为________。
(4) 如果缩小容器容积(温度不变),达到新平衡时混合气体的密度________、平均相对分子质量________。(两空均选填“增大”、“减小”或“不变”)。
(5)如果上述反应在相同条件下从逆反应开始进行,开始加C和D各4/3 mol,要使平衡时各物质的质量分数与原平衡时相等,则还应加入________mol B物质。
(7分)有A、B、C、D四种无色溶液。它们的溶质分别是Na2CO3、Na2SO4、NaHSO4、BaCl2中的一种,为了确定各是何种溶液进行了下列实验,记录为:①A+D―→溶液+气体,②B+C―→溶液+沉淀,③B+A―→溶液+沉淀X,④D+B―→溶液Y+沉淀,⑤溶液Y+沉淀X―→溶液+气体。
(1)根据以上记录确定:A________、B________、C________、D________
(填化学式)。
(2)写出①、③、⑤各反应的离子方程式:
①____________________________________________________;
③___ _________________________________________________;
_________________________________________________;
⑤____________________________________________________。
晶体的世界丰富多彩,晶体的结构纷繁复杂。人教版课程标准高中教材《选修3》向我们展示了一些典型晶体的结构及性质的相关知识,如:干冰、冰、金刚石、石墨、钋、钾、镁、铜、NaCl、CsCl、CaF2。下图是一个立方晶胞图,请大家在上述所列物质范围内回答下列问题:
(1)描述晶体结构的单元叫做晶胞,整块晶体可以看作是数量巨大的晶胞而成的。
( 2)某分子晶体的晶胞如上图(B、C球所代表的位置无该分子)所示,则该分子晶体是;该分子晶体中,一个分子周围紧邻个分子。
2)某分子晶体的晶胞如上图(B、C球所代表的位置无该分子)所示,则该分子晶体是;该分子晶体中,一个分子周围紧邻个分子。
(3)若上图是NaCl的晶胞图,则A球代表,B球代表,C球代表。
(4)若上图是金刚石的晶胞图,则碳原子处于位置(选填“A球”、“B球”、“C球”)。
(5)某金属晶体的晶胞如上图(A、C球所代表的位置无该金属原子)所示,则该金属晶体是。
已知硼酸(分子式为H3BO3)对人体的受伤组织有缓和和防腐作用,故可以用于医药和食品防腐等方面。试回答下列问题:
(1)已知硼酸分子中H只与O成键,则其分子结构式为,由其结构可推知硼酸应属于酸(选填“弱”或“强”)。
(2)已知硼酸晶体呈片状,具有类似石墨那样的片层结构,片层之间作用较弱,有滑腻感,可做润滑剂。则层内H3BO3分子之间的作用力是,层与层间的作用力是。
(3)已知0.01mol硼酸可以被20mL 0.5mol·L-1NaOH溶液恰好完全中和,据此推知硼酸属元酸。研究表明:在大多数情况下,元素的原子在形成分子或离子时,其最外层有达到8电子稳定结构的趋向,如 。写出硼酸与NaOH溶液反应的离子方程式:。
。写出硼酸与NaOH溶液反应的离子方程式:。