有机合成在现代工、农业生产中占有相当重要的地位,有机物F是一种高分子化合物,可作增塑剂,H是除草剂的中间产物,它们的合成路线如下:
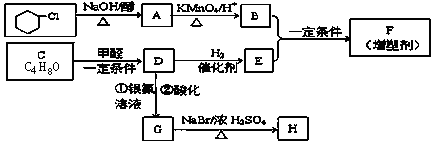
已知:① (R1、R2代表烃基)
(R1、R2代表烃基)
|
②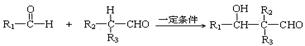
(9分)有A、B、C三种晶体,分别由C、H、Na、Cl四种元素中的一种或几
种形成,对这3种晶体进行实验,结果如下表所示:
| 项目 |
熔点/℃ |
硬度 |
水溶性 |
导电性 |
水溶液与Ag+反应 |
| A |
811 |
较大 |
易溶 |
水溶液(或熔融)导电 |
白色沉淀 |
| B |
3 500 |
很大 |
不溶 |
不导电 |
不反应 |
| C |
-114.2 |
很小 |
易溶 |
液态不导电 |
白色沉淀 |
(1)晶体的化学式分别为:
A:___________________,B:___________________,C:___________________。
(2)晶体的类型分别为:
A:_______________________,B:_______________________,
C:_______________________。
(3)晶体中粒子间的作用分别为
A:_______________________,B:_______________________,
C:_______________________。
(8分)有下列八种晶体:
| A.水晶 | B.冰醋酸 | C.氧化镁 | D.白磷 E.晶体氩 F.氯化铵 G.过氧化钾 H.金刚石 |
(1)属于原子晶体的化合物是_______________,直接由原子构成的晶体是
________________,直接由原子构成的分子晶体是________________。
(2)由极性分子构成的晶体是________________,含有共价键的离子晶体是
_______________,属于分子晶体的单质是________________。
(3)受热熔化后化学键不发生变化的是_______________,需克服共价键的是
__________ ____。
(7分)固体A的化学式为NH5,它的所有原子的最外层都符合相应的稀有气体原子的电子层结构,该物质适当加热就分解成两种气体,试完成:
(1)固体A属于________________晶体,它的电子式为________________。
(2)A溶于水后溶液呈性________________ (填“酸”“碱”或“中”),其原因是(用化学方程式表示) ______________________________________________________________________________。
(3)A与铜或铜的某些化合物在一定条件下可合成CuH,CuH是一种难溶物,它能在氯气中着火,还能与盐酸反应放出气体,请写出这两种反应的化学方程式______________________。
现有前四周期中的A、B、C、D、E五种主族元素,A的最高价氧化物含A40%,A原子中质子数等于中子数;B是第四周期中除稀有气体外原子半径最大的元素;B和D能形成BD型离子化合物,且B、D两离子的电子层结构相同;C和D能形成CD3的化合物;C原子比E原子多1个电子;1.8 g C与足量的稀H2SO4反应,所产生的氢气在标准状况下的体积为2.24 L;C原子中质子数比中子数少1;D原子比A原子多1个质子。则:
(1)五种元素的元素符号分别为:A,B,C,D,E。
(2)五种元素中,单质还原性最强的是,简单离子还原性最强的是。
(3)依次写出A~E五种元素最高价氧化物对应水化物的化学式:、、、、,其中酸性最强的是,碱性最强的是。
(4)D单质与B的最高价氧化物的水化物反应的离子方程式: 。
(5)B、C元素的最高价氧化物的水化物之间反应的化学方程式: 。
下表是元素周期表的一部分
| ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
| 1 |
① |
||||||
| 2 |
② |
③ |
④ |
⑤ |
⑥ |
||
| 3 |
⑦ |
⑧ |
⑨ |
⑩ |
(1)表中元素⑩的氢化物的化学式为 ,此氢化物的还原性比元素⑨的氢化物的还原性 (填“强”或“弱”)。
(2)某元素原子的核外p电子数比s电子数少1,则该元素的元素符号是 ,其单质的电子式为 。
(3)俗称为“矾”的一类化合物通常含有的共同的元素是 。
(4)已知某些不同族元素的性质也有一定的相似性,如元素③与元素⑧的氢氧化物有相似的性质。写出元素③的氢氧化物与NaOH溶液反应的化学方程式
,又如表中与元素⑦的性质相似的不同族的元素是 (填元素符号)。