下列叙述中正确的是
| A.向含有CaCO3沉淀的水中通入CO2至沉淀恰好溶解,再向溶液中加入NaHCO3饱和溶液,又有CaCO3沉淀生成 |
| B.向Na2CO3溶液中逐滴加入(含)等物质的量(HCl)的稀盐酸,生成的CO2与原Na2CO3的物质的量之比为1∶2 |
| C.等质量的NaHCO3和Na2CO3分别与足量盐酸反应,在同温同压下,生成的CO2体积相同 |
| D.向Na2CO3饱和溶液中通入CO2,有NaHCO3结晶析出 |
在密闭的容器中进行如下的反应:
,在温度
和
时,产物的量彧时间的关系如下图所示,符合图象的正确的判断是()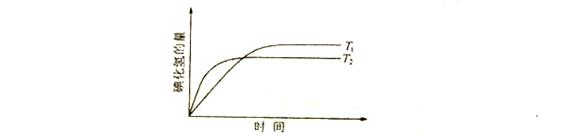
| A. | > , >0 | B. | > , <0 |
| C. | < , >0 | D. | < , <0 |
、
、
三种气体,取
和
按1:1的物质的量之比混合,放入密闭容器中发生如下反应:
+2
 2
,达到平衡后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为3:2,则
的转化率最接近于()
2
,达到平衡后,测得混合气体中反应物的总物质的量与生成物的总物质的量之比为3:2,则
的转化率最接近于()
| A. | 33% | B. | 40% | C. | 50% | D. | 65% |
在相同温度和压强下,对反应CO2(g)+H2(g) CO(g)+H2O(g)进行甲、乙、丙、丁四组实验,实验起始时放入容器内各组分的物质的量见下表
CO(g)+H2O(g)进行甲、乙、丙、丁四组实验,实验起始时放入容器内各组分的物质的量见下表
 |
CO2 |
H2 |
CO |
H2O |
| 甲 |
amol |
amol |
0mol |
0mol |
| 乙 |
2amol |
amol |
0mol |
0mol |
| 丙 |
0mol |
0mol |
amol |
amol |
| 丁 |
amol |
0mol |
amol |
amol |
上述四种情况达到平衡后,n(CO)的大小顺序是( )
| A.乙=丁>丙=甲 | B.乙>丁>甲>丙 |
| C.丁>乙>丙=甲 | D.丁>丙>乙>甲 |
对于反应
 ,能增大正反应速率的措施是()
,能增大正反应速率的措施是()
| A. | 通入大量 | B. | 增大窗口容积 |
| C. | 移去部分 | D. | 降低体系温度 |
碘钨灯比白炽灯使用寿命长。灯管内封存的少量碘与使用过程中沉积在管壁上的钨可以发生反应:W(s)+I2(g) WI2(g)
(温度
)。下列说法正确的是()
WI2(g)
(温度
)。下列说法正确的是()
| A. | 灯管工作时,扩散到灯丝附近高温区的 会分解出 重新沉积到灯丝上 |
| B. | 灯丝附近温度越高, 的转化率越低 |
| C. | 该反应的平衡常数表达式是 |
| D. | 利用该反应原理可以提纯钨 |