已知1mol CO气体完全燃烧生成CO2气体,放出283KJ热量,1mol氢气完全燃烧生成液态水放出286KJ热量,1mol CH4气体完全燃烧生成CO2气体和液态水放出890KJ热
(1)写出H2燃烧热的热化学方程式 。
(2)若1mol CH4气体完全燃烧生成CO2气体和水蒸汽,放出热量 890KJ(填“=”、“>”“<”)
(3)若将a mol CH4,CO,H2混合气体完全燃烧,生成CO2气体和液态水,则放出热量(Q)的取值范围是 。
(4)若将a mol CH4,CO,H2混合气体完全燃烧,生成CO2气体和液态水,且CO2和H2O物质的量相等,则放出热量(Q)的取值范围是 。
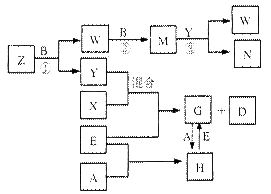 A、B、C、D、E是中学化学常见的五种单质,已知A、B、C、D在常温下均为气态,E为金属,其中D能分别跟A、B、C在一定条件下化合,生成对应的化合物X、Y、Z,其中常温下,Y为液体,X、Z为气体。有关的转化关系如下图所示(反应条件均已略去)。
A、B、C、D、E是中学化学常见的五种单质,已知A、B、C、D在常温下均为气态,E为金属,其中D能分别跟A、B、C在一定条件下化合,生成对应的化合物X、Y、Z,其中常温下,Y为液体,X、Z为气体。有关的转化关系如下图所示(反应条件均已略去)。
(1)化合物Z的空间构型为;构成A的元素的最高价氧化物水化物的化学式为;实验室贮存N的方法是。
(2)写出反应②的化学反应方程式;G→H的离子方程式。
(3)常温下,D与A反应生成1 mol X时放热92.3kJ,写出该反应的热化学方程式:
。
(4)将过量的E加入N的稀溶液中,若反应过程中转移电子的数目为3.01×1023,则参加反应的E的质量为g。
已知:G是一种常用的药用有机物,合成路线如图所示:
①有机物A和C都能与FeCl3发生显色反应,且取代基处于邻位
②有机物G只含碳、氢、氧元素且式量小于200,氧元素的质量分数为35.56%。
请回答:
(1)写出A、C、K的结构简式A________C________K__________
(2)反应①~⑨中,属于取代反应的有______________(填序号)
(3)写出F的常见同分异构体与F在浓硫酸条件下的反应_____________________
(4)写出G在加热条件下与NaOH溶液反应的化学方程式_______________________
(5)写出反应⑥的方程式____________________。
萝卜中具有较多的胡萝卜素,它是人体的主要营养之一。α-胡萝卜素的结构为: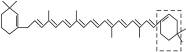
(1)写出α-胡萝卜素的分子式________。
(2)1 mol胡萝卜素最多能与________ mol Br2反应。
(3)β-胡萝卜素与α-胡萝卜素互为同分异构体,且只是虚线框内部分不同,但碳的骨架相同,写出β-胡萝卜素方框内可能的结构简式:______________________。
A、B两种烃通常状况下均为气态,它们在相同状况下的密度之比为1∶3.5。若A完全燃烧,生成CO2和H2O的物质的量之比为1∶2,则A的分子式是________,B的分子式是________。
某烃A 0.2 mol在O2中充分燃烧时,生成化合物B、C各1.2 mol。试完成下列问题:
(1)烃A的分子式为________,B、C的分子式分别是________,________。
(2)若一定量的烃A燃烧后生成B和C各3 mol,则有________g烃A参加了反应,燃烧时消耗标准状况下O2________L。
(3)若烃A不能因反应而使溴水褪色,在一定条件下能与Cl2发生取代反应,其一氯代物只有一种,则烃A的结构简式为___________。