如图装置(Ⅰ)为一种可充电电池的示意图,其中的离子交换膜只允许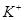 通过,该电池放电时的化学方程式为:
通过,该电池放电时的化学方程式为: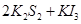 =
=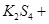 3KI。装置(Ⅱ)为电解示意图,当闭合开关K时,电极X附近溶液先变红。则闭合K时,下列说法正确的是( )
3KI。装置(Ⅱ)为电解示意图,当闭合开关K时,电极X附近溶液先变红。则闭合K时,下列说法正确的是( ) 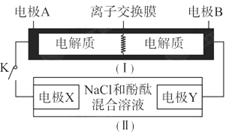
A.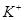 从右到左通过离子交换膜 从右到左通过离子交换膜 |
B.电极A上发生的反应为: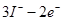 = =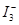 |
C.电极X上发生的反应为: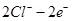 = =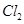 ↑ ↑ |
D.当有0.1 mol 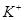 通过离子交换膜,X电极上产生1.12 L气体(标准状况) 通过离子交换膜,X电极上产生1.12 L气体(标准状况) |
下列说法错误的是
A.已知298K时,2SO2(g)+O2(g)  2SO3(g) △H=-197kJ/ mol,对该热化学方程式理解为:在该条件下,向密闭容器中通入2摩SO2和1摩O2,达到平衡时放出热量是197 kJ 2SO3(g) △H=-197kJ/ mol,对该热化学方程式理解为:在该条件下,向密闭容器中通入2摩SO2和1摩O2,达到平衡时放出热量是197 kJ |
| B.CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)===2CO(g)+O2(g)反应的△H=+(2×283.0)kJ/mol |
| C.吸热反应是指反应物所具有的总能量低于生成物所具有的总能量,而不是看反应过程是否需要加热 |
| D.对下列反应:HCl(aq) + NaOH(aq)="NaCl(aq)" + H2O(l)△H=-Q1kJ/mol |
 H2SO4(浓)+NaOH(aq)=
H2SO4(浓)+NaOH(aq)=  Na2SO4(aq)+H2O(l)△H=-Q2kJ/mol
Na2SO4(aq)+H2O(l)△H=-Q2kJ/mol
上述反应均在溶液中进行,则Q2>Q1
下列说法正确的是
A.CH4(g) +  O2(g) ==CO2(g) +2H2O(g) ΔH ==-akJ·mol—1,这里ΔH代表燃烧热 O2(g) ==CO2(g) +2H2O(g) ΔH ==-akJ·mol—1,这里ΔH代表燃烧热 |
| B.CO是不稳定的氧化物,它能继续和氧气反应生成稳定的CO2,所以CO的燃烧反应一定是吸热反应 |
| C.在25℃、101kPa,1molS和2molS的燃烧热相等 |
| D.101kPa时,1mol碳燃烧所放出的热量为碳的燃烧热 |
以NA代表阿伏加德罗常数,则关于热化学方程式
C2H2(g)+ 5/2 O2(g)=2CO2(g)+H2O(l) △H =—1300kJ/mol的说法中,正确的是
| A.有10NA个电子转移时,该反应放出1300kJ的能量 |
| B.有NA个水分子生成且为液体时,吸收1300kJ的能量 |
| C.有4NA个碳氧共用电子对生成时,放出1300kJ的能量 |
| D.有8NA个碳氧双键生成时,放出1300kJ的能量 |
可以判断油脂皂化反应基本完成的现象是
| A.反应液使红色石蕊试纸变成蓝色 | B.反应液使蓝色石蕊试纸变成红色 |
| C.反应后静置,反应液分为两层 | D.反应后静置,反应液不分层 |
某药物结构简式如下图,该物质1 mol与足量NaOH溶液反应,消耗NaOH的物质的量为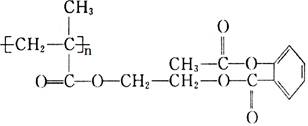
| A.3 mol | B.4 mol | C.3n mol | D.4n mol |