合成氨工业对国民经济和社会发展具有重要的意义。对于密闭容器中的反应:N2(g)+3H2(g)==2NH3(g) 673K,30MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是( )
| A.点a的正反应速率比点b的大 |
| B.点 c处反应达到平衡 |
| C.点d (t1时刻) 和点 e (t2时刻) 处n(N2)不一样 |
| D.其他条件不变,773K下反应至t1时刻,n(H2)比上图中d点的值大 |
实验室有下列试剂:①NaOH溶液②水玻璃③Na2S溶液④Na2CO3溶液⑤NH4Cl溶液⑥澄清石灰水⑦浓H2SO4,其中必须用带橡胶塞的试剂瓶的是()
| A.①⑥ | B.①②③④⑥ |
| C.①②③⑥ | D.①②③④ |
下列粒子在溶液中能大量共存的是()
A. 、Fe2+、 、Fe2+、 、 、 |
B.Fe3+、K+、Cl-、 |
C.Al3+、Na+、 、HS- 、HS- |
D.Ca2+、H+、 、 、 |
叠氮酸(HN3)与醋酸酸性相似,下列叙述中错误的是()
| A.HN3水溶液中粒子浓度大小顺序为:c(HN3)>c(H+)>c(N-3)>c(OH-) |
| B.HN3与NH3作用生成的叠氮酸铵是共价化合物 |
| C.NaN3水溶液中离子浓度大小顺序为:c(Na+)>c(N-3)>c(OH-)>c(H+) |
D. 与CO2含相等电子数 与CO2含相等电子数 |
下列混合溶液中,各离子浓度的大小顺序正确的是()
A.10mL0.1mol·L-1氨水与10mL0.1mol·L-1盐酸混合:c(Cl-)>c( )>c(OH-)>c(H+) )>c(OH-)>c(H+) |
| B.10mL0.1mol·L-1NH4Cl溶液与5mL0.2mol·L-1NaOH溶液混合:c(Na+)=c(Cl-)>c(OH-)>c(H+) |
| C.10mL0.1mol·L-1CH3COOH溶液与5mL0.2mol·L-1NaOH溶液混合:c(Na+)=c(CH3COO-)>c(OH-)>c(H+) |
| D.10mL0.5mol·L-1CH3COONa溶液与6mL1mol·L-1盐酸混合:c(Cl-)>c(Na+)>c(OH-)>c(H+) |
常温下pH=2的一元弱酸HA溶液,其电离百分率为5%,0.01mol·L-1的一元碱BOH溶液中,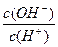 =1×1010。将上述两种溶液等体积混合后,得到溶液中各离子浓度大小关系正确的是()
=1×1010。将上述两种溶液等体积混合后,得到溶液中各离子浓度大小关系正确的是()
| A.c(OH-)>c(H+)>c(B+)>c(A-) | B.c(B+)=c(A-)>c(H+)>c(OH-) |
| C.c(B+)>c(A-)>c(H+)>c(OH-) | D.c(A-)>c(B+)>c(H+)>c(OH-) |