.(1)为了防止水源污染,用简单而又现象明显的方法检验某工厂排放的污水中有无苯酚,此方法是 。
从废水中回收苯酚的方法是:①用有机溶剂萃取废液中的苯酚;②加入某种药品的水溶液使苯酚与有机溶剂脱离;③通入某物质又析出苯酚。试写出②③步的化学反应方程式:
、 。
(2)处理含苯酚的工业废水的流程如下: 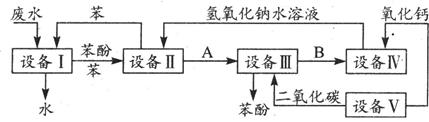
①在设备Ⅳ中,物质B的水溶液和CaO反应后,产物是NaOH、H2O和 。
通过 (填写操作名称)操作,可以使产物相互分离。
②上面流程中,能循环使用的物质是C6H6、CaO、 、 。
(3)为测定废水中苯酚的含量,取此废水100mL,向其中滴加溴水至不再产生沉淀为止,得到沉淀0.331g,求此废水中苯酚的含量(mg/L)是 。
【化学——选修3物质结构与性质】A,B,C,D,E五种元素,均位于周期表的前四周期,它们的核电荷数依次增加,且核电荷数之和为57;B原子的L层P轨道中有2个电子,C的原子核外有三个未成对电子,D与B原子的价电子数相同,E原子的K层电子数与最外层电子数之比为2:1,其d轨道处于全充满状态。
(1)B,D可分别与A形成只含一个中心原子的共价化合物X和Y,其中X的电子式为 ;Y采取的杂化轨道类型为;C与A形成的常见化合物的分子构型为。
(2)B和D的最高价氧化物的晶体中熔点较高的是(填化学式),其原因。
(3)B与C比较电负性较大的是(填元素符号),E2+的核外电子排布式为。
(4)E2+与C的常见氢化物形成的配离子的离子反应方程式为。
(5)铝单质的晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。若已知铝原子半径为d,NA表示阿伏加德罗常数,摩尔质量为M,则该原子的配位数,该晶体的密度可表示为______________,据下图计算,Al原子采取的面心立方堆积的空间利用率为 __________。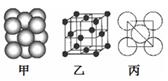
【化学——选修2化学与技术】明矾石经处理后得到明矾[KAl(SO4)2·12H2O]。从明矾制备Al、K2SO4、和H2SO4的工艺过程如下所示: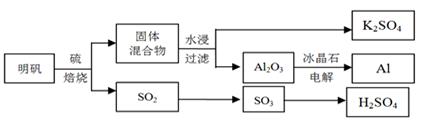
焙烧明矾的化学方程式为:4KAl(SO4)2·12H2O + 3S ="==" 2K2SO4 + 2Al2O3 + 9SO2 + 48H2O
请回答下列问题:
(1)在焙烧明矾的反应中,还原剂是。
(2)从水浸后的滤液中得到K2SO4晶体的方法是。
(3)Al2O3在一定条件下可制得AlN,其晶体结构如图所示,该晶体中Al的配位数是。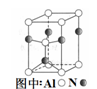
(4)以Al和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,该电池反应的化学方程式是。
(5)焙烧产生的SO2可用于制硫酸。已知25℃、101kPa时:
2SO2(g)+ O2(g)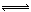 2SO3(g) △H1 = -197 kJ /mol;
2SO3(g) △H1 = -197 kJ /mol;
H2O(g)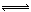 H2O(l)△H2 = -44 kJ/mol;
H2O(l)△H2 = -44 kJ/mol;
2SO2(g)+ O2(g)+ 2H2O(g)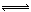 2H2SO4(aq) △H3 = -545 kJ/mol。
2H2SO4(aq) △H3 = -545 kJ/mol。
则SO3(g)与H2O(l)反应的热化学方程式是。
焙烧948 t明矾(M =" 474" g/mol),若SO2的利用率为96%,可产生质量分数为98%的硫酸______t。
甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1)工业上一般采用两种方法制备甲醇:
反应Ⅰ:CO(g) + 2H2 (g) CH3OH (g)
CH3OH (g) H1
H1
反应Ⅱ:CO2(g)+ 3H2(g) CH3OH (g)+H2O(g)
CH3OH (g)+H2O(g) H2
H2
①下表所列数据是反应Ⅰ在不同温度下的化学平衡常数(K)
| 温度 |
250℃ |
300℃ |
350℃ |
| K |
2.041 |
0.270 |
0.012 |
由表中数据判断H1_______________0(填“>”、“=”或“<”)。
②某温度下,将2molCO和6molH2充入2L密闭容器中充分反应,4分钟后反应达到平衡,测得CO的物质的量为0.4mol,则CO的反应速率为______________,此时的压强是反应前压强的___________倍。
(2)反应Ⅱ的平衡常数表达式为____________________,为了加快反应Ⅱ的反应速率,并且提高H2的转化率,采取的措施是_______________(填写正确选项的字母)。
a.增大CO2的浓度 b.增大H2的浓度
c.增大压强d.加入催化剂
(3)工业上利用CO与水蒸气的反应,将有毒的CO转化为无毒的CO2,书写有关热化学反应方程式_______。该反应在830K下进行时,初始浓度到达平衡的时间有如下的关系:
| CO的初始浓度(mol/L) |
2 |
4 |
1 |
3 |
| H2的初始浓度(mol/L) |
3 |
2 |
3 |
3 |
| 时间(min) |
8 |
6 |
12 |
n |
则n 为________min。
(4)近年来,科研人员新开发出一种甲醇和氧气以强碱溶液为电解质溶液的新型手机电池。该电池中甲醇发生反应的一极为______极、其电极反应式为_________________。
(5)用该电池作电源,用惰性电极电解饱和NaCl溶液时,每消耗0.2mol CH3OH,阴极产生标况下气体的体积为L。
选做【化学—有机化学基础】呋喃酚是合成农药的重要中间体,其合成路线如下:
(1)A物质核磁共振氢谱共有个峰,B→C的反应类型是。
(2)已知x的分子式为C4H7C1,写出A→B的化学方程式:。
(3)Y是X的同分异构体,分子中无支链且不含甲基,则Y的名称(系统命名)是。
(4)下列有关化合物C、D的说法正确的是。
①可用氯化铁溶液鉴别C和D②C和D含有的官能团完全相同
③C和D互为同分异构体④C和D均能使溴水褪色
(5)E的同分异构体很多,写出一种符合下列条件的芳香族同分异构体的结构简式:。
①环上的一氯代物只有一种②含有酯基③能发生银镜反应
碳氧化物、氮氧化物、二氧化硫的处理与利用是世界各国研究的热点问题。
(1)消除汽车尾气中的NO、CO,有利于减少PM2.5的排放。已知如下信息:
I.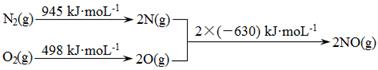
II.N2(g)+ O2(g)  2NO(g)ΔH1
2NO(g)ΔH1
2CO(g) + O2(g) 2CO2 (g) ΔH2=" -565" kJ·mol-1
2CO2 (g) ΔH2=" -565" kJ·mol-1
①ΔH1=。
②在催化剂作用下NO和CO转化为无毒气体,写出反应的热化学方程式。
(2)电化学气敏传感器法测定汽车尾气。其中CO传感器的工作原理如图所示,则工作电极的反应式为
(3)工业上可以用NaOH溶液或氨水吸收过量的SO2,分别生成NaHSO3、NH4HSO3,其水溶液均呈酸性。相同条件下,同浓度的两种酸式盐的水溶液中c(SO32-)较小的是,用文字和化学用语解释原因。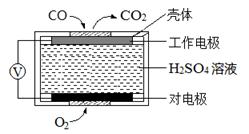
(4)T℃时,在 2L恒容密闭容器中,加入Fe3O4、CO各1.0 mol ,10 min反应达到平衡时,容器中CO2的浓度是0.4 mol /L。
①能证明该反应达到化学平衡的是(选填字母)。
a.容器内压强不再变化 b.容器内CO、CO2物质的量比为1 : 1
c.容器内气体的质量不再变化 d.生成CO2的速率与消耗CO的速率相等
②l0 min内,反应的平均反应速率v (CO2)=。
③T℃时,该反应的平衡常数K=。