(每空2分,共16分)铝镁合金已成为飞机制造、化工生产等行业的重要材料。研究性学习小组的同学,为测定某含镁3%-5%的铝镁合金(不含其它元素)中镁的质量分数,设计下列两种不同实验方案进行探究。填写下列空白。 [方案一]
[方案一] 〖实验方案〗将铝镁合金与足量NaOH溶液反应,测定剩余固体质量。
〖实验方案〗将铝镁合金与足量NaOH溶液反应,测定剩余固体质量。 实验中发生反应的化学方程式是 。
实验中发生反应的化学方程式是 。 〖实验步骤〗
〖实验步骤〗 (1)称取5.4g铝镁合金粉末样品,溶于V mL 2.0 mol/L NaOH溶液中。为使其反应完全,则NaOH溶液的体积V ≥ 。
(1)称取5.4g铝镁合金粉末样品,溶于V mL 2.0 mol/L NaOH溶液中。为使其反应完全,则NaOH溶液的体积V ≥ 。 (2)过滤、洗涤、干燥、称量固体。该步骤中若未洗涤固体,测得镁的质量分数将
(2)过滤、洗涤、干燥、称量固体。该步骤中若未洗涤固体,测得镁的质量分数将  (填“偏高”、“偏低”或“无影响”)。
(填“偏高”、“偏低”或“无影响”)。 [方案二
[方案二
 ]
]
〖实验方案〗将铝镁合金与足量稀硫酸溶液反应,测定生成气体在通常状况(约20℃,1.01 105Pa)的体积。
105Pa)的体积。 〖问题讨论〗(1)同学们拟选用下列实验装置完成实验:
〖问题讨论〗(1)同学们拟选用下列实验装置完成实验:







 ①你认为最简易的装置其连接顺序是:a接( )( )接( )( )接( )(填接口字母,可不填满。)
①你认为最简易的装置其连接顺序是:a接( )( )接( )( )接( )(填接口字母,可不填满。) ②实验开始时,先打开分液漏斗上口的玻璃塞,再轻轻打开分液漏斗可旋转的活塞,一会儿后稀硫酸也不能顺利滴入锥形瓶中。请你帮助分析原因 。
②实验开始时,先打开分液漏斗上口的玻璃塞,再轻轻打开分液漏斗可旋转的活塞,一会儿后稀硫酸也不能顺利滴入锥形瓶中。请你帮助分析原因 。 ③实验结束时,在读取测量实验中生成氢气的体积时,你认为最合理的顺序是 。
③实验结束时,在读取测量实验中生成氢气的体积时,你认为最合理的顺序是 。
A.等待实验装置冷却 |
B.上下移动量筒f,使其中液面与广口瓶中液面相平 |
C.上下移动量筒g,使其中液面与广口瓶中液面相平 |
D.视线与凹液面的最低点水平读取量筒中水的体积 |
 (2)仔细分析实验装置后,同学们经讨论认为以下两点会引起较大误差:稀硫酸滴入锥形瓶中,即使不生成氢气,也会将瓶内空气排出,使所测氢气体积偏大;实验结束时,连接广口瓶和量筒的导管中有少量水存在,使所测氢气体积偏小。于是他们设计了右图所示的实验装置。
(2)仔细分析实验装置后,同学们经讨论认为以下两点会引起较大误差:稀硫酸滴入锥形瓶中,即使不生成氢气,也会将瓶内空气排出,使所测氢气体积偏大;实验结束时,连接广口瓶和量筒的导管中有少量水存在,使所测氢气体积偏小。于是他们设计了右图所示的实验装置。
 ①装置中导管a的作用是 。
①装置中导管a的作用是 。 ②实验前后碱式滴定管中液面读数分别为V1 mL、V2 mL。则产生氢气的体积为_________mL。
②实验前后碱式滴定管中液面读数分别为V1 mL、V2 mL。则产生氢气的体积为_________mL。



下图是实验室制取并收集Cl2的装置。A是Cl2发生装置,E是硬质玻璃管中装有细铁丝网;F为干燥的广口瓶,烧杯G为尾气吸收装置。
试回答:
(1)A中发生的化学反应方程式为。
(2)C、D、G中各装的药品:C__________;D__________;G__________。
(3)E中的现象为;反应方程式为。
(4)写出G中反应的离子方程式。
(5)若将Cl2和SO2等物质的量混合漂白作用减弱,用化学方程式解释原因。
海波(Na2S2O3·5H2O)常用手纺织和造纸工业,海波是无色透明的晶体,易溶于水,遇酸立即分解:S2O32— + 2H+ ="==" S↓+ SO2↑+ H2O。
硫化碱法是工业上制备海波的方法之一,反应原理为:2Na2S+Na2CO3+4SO2 ="==" 3Na2S2O3+CO2
某研究小组在实验室用硫化碱法制备Na2S2O3·5H2O,实验装置如下图所示: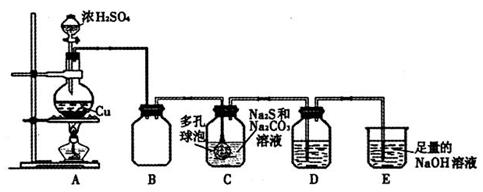
(1)装置A中滴加浓硫酸的仪器名称是,发生反应的化学方程式是,实验室还可以用A装置制取的气体单质有(填化学式)。
(2)装置C中连接多孔球泡可以提高S O2的吸收效率,其依据的原理是。
(3)装置D的作用是检验装置C中SO2的吸收效率,D中的试剂可以是。
a.品红溶液b.氢氧化钠溶液
c.酚酞溶液d.酸性高锰酸钾溶液
(4)装置E的作用是。
(5)实验制得的Na2S2O3·5H2O产品中可能含有Na2SO3、Na2SO4等杂质。请设计实验,检测Na2S2O3·5H2O产品中是否存在Na2SO4杂质,简要说明实验操作、现象和结论:。
(6)Na2S2O3溶液是定量实验中的常用试剂,为了测定某K2Cr2O7溶液的浓度,研究小组的同学准确量取10.00mL K2Cr2O7溶液于锥形瓶中,加入过量KI固体和适量的稀H2SO4,滴加指示剂,用0.1000 mol·L-1 Na2S2O3标准溶液滴定至终点,3次平行实验测得平均消耗Na2S2O3溶液的体积为30.00 mL,则c(K2Cr2O7) =mol·L-1。(已知:Cr2O72— +6I— +14H+="==" 2Cr3+ +3I2 +7H2O,2S2O32— + I2===S4O62—+2 I—)
某待测液中可能含有Ba2+、Fe3+、K+、Fe2+、CO32-、Cl-等离子,进行如下实验:
①取适量待测液于试管中,加入稀H2SO4,有白色沉淀生成;
②过滤,取少量滤液,滴入2滴KSCN溶液,没有明显的现象出现;
③在步骤②中的溶液中,继续滴加氯水,溶液立即变红。
根据实验现象回答:
(1)待测液中一定含有的离子是,一定不含有的离子是;
(2)还有一种离子不能确定是否存在,要确认这种离子的实验方法和现象是。
某学习小组设计了如图所示的实验方案来制取次氯酸钠和探究氯水的性质。
图中:①为氯气发生装置;②试管里盛有15 mL 8% NaOH溶液,并置于冰水浴中;
③试管里是滴有酚酞的NaOH溶液;④为尾气吸收装置。
请填写下列空白:
(1)实验前必须对整套装置进行的操作是;
(2)制取氯气时,在烧瓶里加入一定量的二氧化锰,通过__________(填写仪器名称)向烧瓶中加入适量的浓盐酸。实验时为了除去氯气中的氯化氢气体,可在①与②之间安装盛有(填写下列编号字母)的净化装置。
a.碱石灰b.饱和食盐水
c.浓硫酸d.饱和碳酸氢钠溶液
(3)写出②装置中发生的离子反应方程式;
(4)实验中可观察到③试管的实验现象是溶液褪色。某同学提出两种猜想:
猜想一:氯气与NaOH溶液发生反应使溶液褪色
猜想二:
请设计实验验证哪种猜想是正确的?
下图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:
(1)该浓盐酸的物质的量浓度为___________mol/L。
(2)某学生欲用上述浓盐酸和蒸馏水配制250 mL物质的量浓度为0.7 mol/L稀盐酸。
①该学生用量筒量取________ mL上述浓盐酸进行配制;
②所需的实验仪器有:①胶头滴管、②烧杯、③量筒、④玻璃棒,配制稀盐酸时,还缺少的仪器有。
③下列操作导致所配制的稀盐酸的物质的量浓度偏低的是(填字母)。
| A.用量筒量取浓盐酸时俯视凹液面 |
| B.未恢复到室温就将溶液注入容量瓶并进行定容 |
| C.容量瓶用蒸馏水洗后未干燥 |
| D.定容时仰视液面 |
E、未洗涤烧杯和玻璃棒
(3)若在标准状况下,将a L HCl气体溶于1 L水中,所得溶液密度为d g/mL,则此溶液的物质的量浓度为mol/L。
a. b.
b. c.
c. d.
d.