将40 mL 1.5 mol·L-1的CuSO4溶液与30 mL 3 mol·L-1的NaOH溶液混合生成浅蓝色沉淀,假如溶液中Cu2+或OH-浓度都已变得很小,可忽略,则生成沉淀的组成可表示为( )
| A.Cu(OH)2 | B.CuSO4·Cu(OH)2 | C.CuSO4·2Cu(OH)2 | D.CuSO4·3Cu(OH)2 |
下列五组物质,其中一定互为同分异构体的组是 ( )
①淀粉和纤维素②硝基乙烷 C2H5NO2和甘氨酸NH2CH2COOH③乙酸和乙二酸
④二甲苯和苯乙烯⑤2—戊烯和环戊烷
| A.①② | B.②③④ | C.①③⑤ | D.②⑤ |
下列有机物由浓硝酸发生酯化反应而得到的是()
| A. TNT | B. CH3CH2NO2 | C.硝化甘油 | D. C6H5NO2 |
下列化学用语中正确的是()
| A.乙烯的结构式为CH2CH2 | B.葡萄糖的实验式为CH2O |
C.醛基的电子式: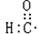 |
D.聚丙烯的结构简式: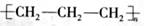 |
有机化学发展成为化学的一个重要分支,渗透到医药、国防、生产的各个角落,在人类认识、研究有机物方面,化学家们不断探索,做出了不可磨灭的贡献。下列说法不正确的是()
| A.德国化学家维勒合成了醋酸,首次打破了有机物和无机物的界限 |
| B.李比希用燃烧法来测定有机化合物中碳氢元素质量分数 |
| C.甲烷与氯气的反应属于自由基型链反应 |
| D.同位素示踪法可用来研究有机化学反应历程 |
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是()
①CH3OH(g)+H2O(g) = CO2(g)+3H2(g) △H =" +" 49. 0 kJ·mol-1
②CH3OH(g)+1/2O2(g) = CO2(g)+2H2(g) △H =-192. 9 kJ·mol-1
下列说法正确的是 ( )
| A.1mol CH3OH充分燃烧放热为192. 9 kJ |
| B.反应①中的能量变化如上图所示 |
| C.CH3OH转变成H2的过程一定要吸收能量 |
| D.根据②推知反应:CH3OH(l) +1/2O2(g) = CO2(g) +2H2(g) △H >-192. 9kJ·mol-1 |