有关下列图像说法正确的是( )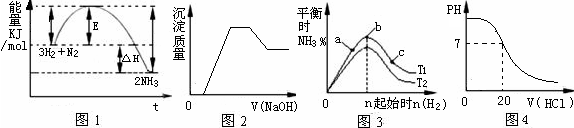
| A.由图1可知合成氨反应为自发反应,加入适当的催化剂,E和△H都减小 |
| B.图2表示向含有H+、Mg2+、Al3+、NH4+中加入NaOH溶液与产生沉淀质量的变化关系 |
| C.图3表示合成氨反应在其他条件不变的情况下,改变起始物n(H2)对此反应平衡的影响。可知反应物N2的转化率最高的是b点;T1>T2,K2> K1(T1和T2表示温度,K1、K2表示对应温度下平衡常数) |
| D.图4表示25℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1氨水的pH随加入盐酸体积的变化 |
某同学做乙醛的性质实验时,取1mol/L的CuSO4溶液和0.5mol/L的NaOH溶液各1mL,在一支洁净的试管内混合后,向其中又加入0.5mL 40%的乙醛,加热煮沸,结果未出现砖红色沉淀。实验失败的原因可能是()
| A.反应温度不够高 | B.加入NaOH溶液的量不够 |
| C.加入乙醛太多 | D.加入CuSO4溶液的量不够 |
由2—氯丙烷制取1,2—丙二醇时,需要经过下列哪几步反应()
| A.加成 → 消去 → 取代 | B.消去 → 加成 → 取代 |
| C.取代 → 消去 → 加成 | D.消去 → 加成 → 消去 |
下列各组物质中,用分液漏斗可以将其分开的是()
| A.甲苯和苯酚 | B.乙醇和乙醛 | C.硝基苯和水 | D.乙酸和乙酸乙酯 |
下列实验式中,无需知道相对分子质量即可确定分子式的是()
| A.CH3O | B.CH | C.CH2O | D.C2H3 |
空气是人类生存所必需的重要资源,为改善空气质量而启动的“蓝天工程”得到了全民的支持。下列措施不利于“蓝天工程”建设的是()
| A.推广使用燃煤脱硫技术,防治SO2污染 |
| B.实施绿化工程,防治扬尘污染 |
| C.研制开发燃料电池汽车,消除机动车尾气污染 |
| D.加大石油、煤炭的开采速度,增加化石燃料的供应量 |