在蒸馏实验中,下列叙述不正确的是
| A.在蒸馏烧瓶中加入约1/3体积的自来水,并放入几粒碎瓷片 |
| B.蒸馏结束时,先停止通冷却水,再熄灭酒精灯 |
| C.冷水从冷凝管的下口入,上口出 |
| D.收集冷凝水时,应弃去开始蒸馏出的部分 |
关于锌铜—稀硫酸原电池的叙述,错误的是
| A.锌是正极,其质量逐渐减小 | B.电流从锌片经导线流向铜片 |
| C.电子从锌片经导线流向铜片 | D.氢离子在铜表面被还原,产生气泡 |
反应 A+B →C(△H <0)分两步进行① A+B→X (△H >0)② X→C(△H <0)下列示意图中,能正确表示总反应过程中能量变化的是: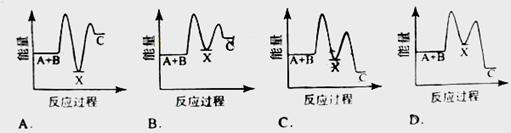
下列有关化学用语使用正确的是:
A.硫离子的结构示意图: |
B.NH4Cl的电子式: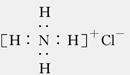 |
| C.原子核内有10个中子的氧原子:18 8O | D.Na2O2的电子式为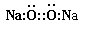 |
下列与化学反应能量变化相关的叙述正确的是:
| A.生成物总能量一定低于反应物总能量 |
| B.放热反应的反应速率总是大于吸热反应的反应速率 |
| C.应用盖斯定律,可计算某些难以直接测量的反应焓变 |
| D.同温同压下, H2(g)+ Cl2(g)==="2HCl(g)" 在光照和点燃条件下反应的ΔH不同 |
下面均是正丁烷与氧气反应的热化学方程式(25℃,101 kPa):
①C4H10(g)+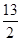 O2(g)===4CO2(g)+5H2O(l)ΔH=-2878 kJ/mol
O2(g)===4CO2(g)+5H2O(l)ΔH=-2878 kJ/mol
②C4H10(g)+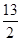 O2(g)===4CO2(g)+5H2O(g)ΔH=-2658 kJ/mol
O2(g)===4CO2(g)+5H2O(g)ΔH=-2658 kJ/mol
③C4H10(g)+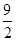 O2(g)===4CO(g)+5H2O(l)ΔH=-1746 kJ/mol
O2(g)===4CO(g)+5H2O(l)ΔH=-1746 kJ/mol
④C4H10(g)+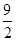 O2(g)===4CO(g)+5H2O(g)ΔH=-1526 kJ/mol
O2(g)===4CO(g)+5H2O(g)ΔH=-1526 kJ/mol
由此判断,正丁烷的燃烧热是:
| A.-2878 kJ/mol | B.-2658 kJ/mol |
| C.-1746 kJ/mol | D.-1526 kJ/mol |