(12分)今年5月我区举行实验技能考查,某兴趣小组的同学在帮助老师准备化学实验时,发现实验台上整齐摆放的药品中(见下图),有一试剂瓶的标签破损。为了鉴定该试剂成分,同学们做了以下探究:
【提出问题】这瓶试剂的成分是什么?
[讨论]根据受损标签及实验室药品分类摆放的原则,这瓶试剂可能不是_______________________;
A.酸 B.碱 C.盐
[猜想]①可能是NaOH溶液;②可能是Na2CO3溶液;
③可能是_______________________(写一种)。
[探究活动]
(1)小军取少量试样于小试管中,滴加酚酞试液,溶液变为红色。由此小军认为猜想①正确。
经同学们交流讨论后,一致认为小军的方案不可行,理由是_______________________
(2)小华同学认为,虽然小军的实验不能得到正确的结论,但只要再往溶液中滴加一种氯化
物溶液,同样能得出正确的结论。
| 操作步骤 |
实验现象 |
实验结论 |
| 取少量滴有酚酞试液的试样于小试管中,滴加足量的___________ |
溶液由红色褪为无色 且有白色沉淀产生 |
猜想②正确 |
(3)小亮发现要进一步确定(1)中的成分,只需选择上图已有的试剂就能把它鉴定出来。于是他们进行了如下实验。
| 操作步骤 |
实验现象 |
结论及化学方程式 |
| 取少量试样于小试管中,滴加适量的_______________________ |
_________________ _________________ |
猜想②正确 有关化学方程式 _________________ |
[实验反思]实验室盛放NaOH溶液的试剂瓶不能用玻璃塞,其原因是:NaOH与玻璃中的
SiO2发生反应,其化学方程式为2NaOH + SiO2=" X" + H2O,产物X使瓶口与塞子粘合在一起。
试推测X的化学式为_________________。
实验室制取SO2的反应原理为:Na2SO3+H2SO4(浓)==Na2SO4+SO2↑+H2O。
请用下列装置设计一个实验,以测定SO2转化为SO3的转化率:
转化率=
二氧化硫熔点(℃):-72.7,沸点(℃):-10
三氧化硫熔点(℃):16.8,沸点(℃):44.8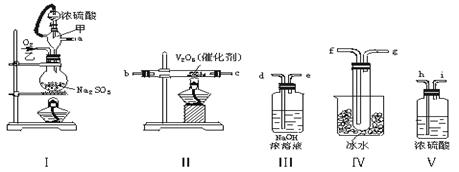
(1)这些装置的连接顺序(按气体左右的方向)是
→→→→→→→(填各接口的编号)。
(2)实验时甲仪器的作用是。
(3)从乙处均匀通入O2,为使SO2有较高的转化率,实验时Ⅰ处滴入浓硫酸与Ⅱ处加热催化剂的先后顺序是。
(4)Ⅳ处观察到的现象是。
(5)用n mol Na2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,称得Ⅲ处增重mg,则本实验中SO2的转化率为。
NO很容易与许多分子迅速发生反应,科学家发现在生物体中不断地产生NO,用于细胞间传递信息;NO还参与心血管系统、免疫系统以及中枢和外围神经系统的调控。
Ⅰ.(1)实验室用金属铜和稀硝酸制取NO的离子方程式为________________________。
(2)NO是有毒气体,某学生为防止污染,用分液漏斗和烧杯装配了一套简易的、能随开随用、随关随停的NO气体发生装置,如图所示。
①实验室若没有铜丝,而只有小铜粒,在使用上述装置进行实验时,可用丝状材料包裹铜粒以代替铜丝进行实验,这种丝状材料的成分可以是________(填选项编号)。
| A.铁 | B.铝 | C.铂 | D.玻璃 |
②打开分液漏斗的活塞使反应进行,在分液漏斗中实际看到的气体是红棕色的,原因是________(用化学方程式表示)。
(3)以下收集NO气体的装置,合理的是________(填选项代号)。
(4)假设实验中12.8 g Cu全部溶解,需要通入标况下________L O2才能使NO全部溶于水。
Ⅱ.用金属铜制取硝酸铜,从节约原料和防止环境污染的角度考虑,下列4种方法中最好的是________(填“甲”、“乙”、“丙”或“丁”)。
甲:铜 硝酸铜
硝酸铜
乙:铜 硝酸铜
硝酸铜
丙:铜 氯化铜
氯化铜 硝酸铜
硝酸铜
丁:铜 氧化铜
氧化铜 硝酸铜。
硝酸铜。
(1)探究一溴环己烷与NaOH的醇溶液共热发生的是水解反应还是消去反应,甲、乙两位同学分别设计如下两个实验方案:
甲:向反应混合物中滴入稀HNO3中和NaOH,后滴入AgNO3溶液,若有浅黄色沉淀,则可以证明发生了消去反应。
乙:向反应混合物中滴入溴水,若溶液颜色很快褪去,则可证明发生了消去反应。请评价上述两个方案是否合理,并说明理由。
甲:_________,______________________________________________________。
乙:_________,______________________________________________________。
(2)如图所示为实验室制取少量硝基苯的装置.根据题意完成下列填空:
①写出制取硝基苯的化学方程式_______________________。
②长玻璃导管的作用是_______________________。
③硝基苯有毒,如果少量的液体溅在皮肤上,应用擦洗.
| A.苯 | B.酒精 | C.硫酸 | D.水. |
(3)某实验小组用下列装置进行乙醇催化氧化的实验.
甲和乙两个水浴作用不相同.甲的作用是;
乙的作用是______________。
(1)实验室从海带中提取碘的流程如下:
①在进行实验b的过程中,可以选择的有机溶剂是__________。
A.酒精B.四氯化碳 C.苯
②从I2的有机溶液中提取碘的装置如图1所示,请指出仪器d的名称____。冷凝管中的水流方向是(填“由e至f”或“由f至e”)
(2)图2是实验室制取乙酸乙酯的实验装置,回答下列问题:
①在A试管中加入试剂的顺序是。
A.先浓硫酸再乙醇后乙酸
B.先浓硫酸再乙酸后乙醇
C.先乙醇再浓硫酸后乙酸
②在试管B中常加入________(填写试剂)来接收乙酸乙酯,分离出乙酸乙酯的主要仪器是。
某研究性小组探究乙酸乙酯的反应机理,实验如下:已知:相关物理性质(常温常压)
| 密度g/mL |
熔点/℃ |
沸点/℃ |
水溶性 |
|
| 乙醇 |
0.79 |
-114 |
78 |
溶 |
| 乙酸 |
1.049 |
16.2 |
117 |
溶 |
| 乙酸乙酯 |
0.902 |
−84 |
76.5 |
不溶 |
合成反应:在三颈烧瓶中加入乙醇5mL,硫酸5mL,2小片碎瓷片。漏斗加入乙酸14.3 mL,乙醇20 mL。冷凝管中通入冷却水后,开始缓慢加热,控制滴加速度等于蒸馏速度,反应温度不超过120 ℃。分离提纯:将反应粗产物倒入分液漏斗中,依次用少量饱和的Na2CO3溶液、饱和NaCl溶液、饱和CaCl2溶液洗涤,分离后加入无水碳酸钾,静置一段时间后弃去碳酸钾。最终通过蒸馏得到纯净的乙酸乙酯。
回答下列问题:
(1)制取乙酸乙酯化学方程式为:____________________。
(2)浓硫酸与乙醇如何混合?。
(3)如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是_______(填正确答案标号)。
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(4)控制滴加乙酸和乙醇混和液的速度等于蒸馏速度目的是?。
(5)蒸出的粗乙酸乙酯中主要有哪些杂质?。
(6)饱和的Na2CO3溶液洗涤除去乙酸,能否换成NaOH溶液?若不能,为什么?(用化学方程式表示);。
用饱和NaCl溶液洗涤除去残留的Na2CO3溶液,为什么不用水?。