在温度不变下,在恒压容器a与恒容容器b中,分别充入体积比为1∶3的N2和H2。若开始时两容器的体积相等,且在相同条件下达到平衡时,两容器中N2的转化率应当是
| A.a中大 | B.b中大 | C.a、b中一样大 | D.无法判断 |
可以充分说明反应P(g)+Q(g)  R(g)+S(g)在恒温下已达到平衡的是
R(g)+S(g)在恒温下已达到平衡的是
| A.反应容器内的压强不随时间改变 |
| B.反应容器内P、Q、R、S四者浓度之比为1:1:1:1 |
| C.P的生成速率和S的生成速率相等 |
| D.反应容器内的气体总物质的量不随时间变化 |
若pH=3的酸溶液和pH=11的碱溶液等体积混合后溶液呈酸性,其原因可能
| A.生成一种强酸弱碱盐 | B.弱酸溶液和强碱溶液 |
| C.强酸与弱碱溶液反应 | D.一元强酸溶液与一元强碱溶液反应 |
在一密闭容器中进行如下反应:2SO2(气)+O2(气) 2SO3(气),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2mol/L、0.1mol/L、0.2mol/L,当反应达平衡时,可能存在的数据是
2SO3(气),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2mol/L、0.1mol/L、0.2mol/L,当反应达平衡时,可能存在的数据是
| A.SO2为0.4mol/L、O2为0.2mol/L | B.SO2为0.25mol/L |
| C.SO2、SO3均为0.15mol/L | D.SO3为0.4mol/L |
随着人们生活质量的不断提高,废电池必须集中处理的问题被提到议事日程,首要原因是
| A.利用电池外壳的金属材料 |
| B.防止电池中汞、镉和铅等重金属离子对土壤和水源的污染 |
| C.不使电池中渗泄的电解液腐蚀其他物品 |
| D.回收其中石墨电极 |
相同温度下等物质的量浓度的下列溶液中,pH值最小的是
A.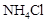 |
B.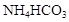 |
C. |
D. |