磷是存在于自然界和生物体内的的重要元素。回答下列与磷及其化合物有关的问题。
(1)磷在自然界里主要以 的形式存在于矿石中,这些磷矿石 溶于水,其中的磷元素 被作物吸收。
(2)磷(相对原子质量为31)在空气中燃烧生成的氧化物通常可用做强干燥剂。制备100g这种干燥剂所消耗的空气的体积约为 L(在标准状况下)。
(3)有机磷农药“乐果”的结构简式是: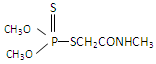 ,其中所含的双键有 个。
,其中所含的双键有 个。
下图为某药物合成路线的一部分。
(1)A→B的化学方程式为,E中的含氧官能团名称为、。
(2)若②的反应历程经历了中间产物 ,则该反应历程先后经历的反应类型为、。试剂X的结构简式为。
,则该反应历程先后经历的反应类型为、。试剂X的结构简式为。
(3)写出两种满足下列要求的D的同分异构体的结构简式,。
①分子中有4种化学环境不同的氢原子;
②可发生水解反应,一种产物可发生银镜反应,另一种能与FeCl3发生显色反应;
③分子中的氯原子不与苯环直接相连。
物质净化对生产生活很重要的意义。
(1)除去水中的 Ca2+,Mg2+等阳离子,完成此目标可使用____(填材料名称)。
(2)催化还原法可以净化硝酸工业尾气,下列物质中不能用于除去尾气中氮氧化物的是________(填字母序号)。
| A.NH3 | B.CH4 | C.CO2 | D.H2 |
(3)接触法制硫酸的工艺中,沸腾炉产生的炉气必须经过净化,除去其中的粉尘和______,净化后的炉气进入_____(填设备名称)。
(4)煤的气化技术的主要产物是______,将煤加热以得到焦炉气、煤焦油及焦炭等产品的技术称为___________ 。
金属钛性能优越,被誉为继Fe、Al后应用广泛的“第三金属”。
(1)写出Ti基态原子的电子排布。
(2)钛能与B、C、N、O等非金属元素形成稳定的化合物。则电负性CB(选填“>”“<”),第一电离能N>O,原因是。
(3)月球岩石玄武岩的主要成分为钛酸亚铁(FeTiO3)。FeTiO3与80%的硫酸反应可生成TiOSO4。SO42-的空间构型为,其中硫原子采用杂化,氧原子的价电子排布图为,任意写出一种SO42-等电子体。
(4)将TiOSO4的稀溶液加热水解后,经进一步反应,可得到钛的某种氧化物。该氧化物的晶胞结构图如图所示。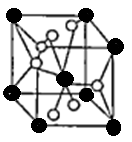
则该氧化物的化学式(图中钛原子用“O”表示。氧原子用“O”表示)
避蚊酯(DMP)是一种塑化剂.相对分子质量为194,摄人后对人体有一定的危害,其结构可表示为 (其中R为烃基)实验室由以下方法可得到DMP
(其中R为烃基)实验室由以下方法可得到DMP
请回答:
(1)物质C中官能团的名称为。
(2)下列有关DMP的说法可能正确的是。(填字母标号)
A.DMP的分子式为C10H12O4
B.DMP可以发生取代、加成、氧化等反应
C.DMP在水中的溶解度不大
(3)B与乙二酸(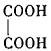 )在一定条件下可以按物质的量1:1发生反应生成高分子化合物,该高分子化合物的结构简式为。
)在一定条件下可以按物质的量1:1发生反应生成高分子化合物,该高分子化合物的结构简式为。
(4)工业上以邻二甲苯(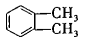 )为原料先生产苯酐(
)为原料先生产苯酐(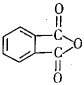 ),再使其与某醇在一定条件下反应制取DMP。苯酐与该醇制取DMP的化学方程式为。
),再使其与某醇在一定条件下反应制取DMP。苯酐与该醇制取DMP的化学方程式为。
(5)芳香化合物E与C互为同分异构体,若lmo E与足量银氨溶液反应最多生成2mol Ag,则E可能的结构简式为。B也存在多种同分异构体,符合下列条件的B的同分异构体有种。
①l mol有机物可以与2mol NaOH反应
②苯环上的一氯代物只有一种。
水处理主要包括水的净化、污水处理、硬水软化和海水淡化等。
(1)水处理技术的核心是减少或除去水中的各种杂质离子。目前________和________是主要的去离子方法。
(2)ClO2是一种性能优良的消毒剂,可将废水中少量的S2-、NO2-和CN-等有毒有害的还原性离子氧化除去。请写出ClO2将废水中剧毒的CN-氧化成无毒气体的离子方程式________。
(3)地下水往往含有钙、镁的碳酸盐,自来水厂需要对地下水进行________处理。把进行过离子交換的CaR2(或MgR2)型树脂置于______中浸泡一段时间后便可再生。
(4)海水的淡化是除去海水中所含的盐分,右面是海水利用电渗析法获得淡水的原理图,已知海水中含有Na+、Cl-、Ca2+、Mg2+、SO42-等离子,电极为惰性电极。请回答: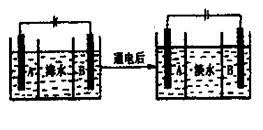
①阳离子交换膜是指________(填“A”或“B”)。
②写出通电后阳极区的电极反应式________________。