某气态烃含C质量分数为85.7%,含H质量分数为14.3%,在标准状况下的密度是2.5g/L。该烃能使酸性高锰酸钾溶液或溴水褪色。求:
(1)该烃的分子式______;
(2)写出它的各种同分异构体的结构简式(不考虑立体异构、顺反异构):____________。
实验室制备硝基苯的主要步骤如下:
①配制一定比例的浓硫酸与浓硝酸的混合酸,加入反应器中。
②向室温下的混合酸中逐滴加入一定质量的苯,充分振荡,混合均匀。
③在50 ℃—60 ℃下发生反应,直至反应结束。
④除去混合酸后,粗产品依次用蒸馏水和5% NaOH溶液洗涤,最后再用蒸馏水洗涤。
⑤将用无水CaCl2干燥后的粗硝基苯进行蒸馏,得到纯硝基苯。完成下列空白:
(1)配制一定比例浓硫酸与浓硝酸混合酸时,操作注意事项是__________________________。
(2)步骤③中,为了使反应在50 ℃—60 ℃下进行,常用的方法是______________________。
(3)步骤④中洗涤、分离粗硝基苯应使用的仪器是_______________________。
(4)步骤④中粗产品用5% NaOH溶液洗涤的目的是______________________。
取0.1 mol苯的同系物完全燃烧后,生成的气体通过浓硫酸,浓硫酸增重10.8 g,再通过氢氧化钾溶液后,气体减轻39.6 g。该苯的同系物在苯环上的一氯代物、二氯代物、三氯代物分别只有一种。根据上述条件,推断它的分子式是___________,结构简式是___________,名称是___________。
有4种无色液态物质:己烯、己烷、苯和甲苯,符合下列各题要求的分别是:
(1)不能与溴水和KMnO4酸性溶液反应,但在Fe屑作用下能与液溴反应的是__________,生成的有机物名称是___________,反应化学方程式为__________,此反应属于__________反应。
(2)不与溴水和KMnO4酸性溶液反应的是___________。
(3)能与溴水和KMnO4酸性溶液反应的是___________。
苯环上原有的取代基对新取代导入苯环上的取代基的位置有一定的影响,其规律是:
(1)苯环上新导入的取代基所占的位置主要决定于原有取代基的性质。
(2)可以把原有取代基分成两类:第一类取代基主要使新导入的取代基进入苯环的邻位和对位,如—OH、—CH3(或烃基)、—Cl、—Br、—O—COR等,第二类取代基主要使新导入的取代基进入苯环的间位。例如—NO2、—SO3H、—CHO等。
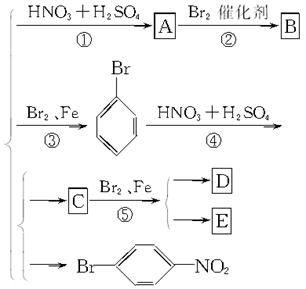
请写出下图中②④⑤三步反应的化学方程式。
二甲苯苯环上的一溴代物有六种同分异构体,这些一溴代物与生成它的对应二甲苯的熔点(℃)分别是
| 一溴代二甲苯 |
234 |
206 |
213.8 |
204 |
214.5 |
205 |
| 对应的二甲苯 |
13 |
-54 |
-27 |
-54 |
-27 |
-54 |
由上述可推断,熔点为234 ℃的一溴代二甲苯的结构简式为_________,熔点为-54 ℃的二甲苯名称为_________。