某混合物X由A12O3、Fe2O3、Cu、SiO2中的一种或几种物质组成。进行如下实验。
请回答:
(1)由I可知X中一定存在的是 ,步骤I所发生反应的离子方程式为: 、 。
(2)反应II的化学方程式是 。
为进一步确定上述混合物X的成分,另取9.4gX进行如下实验。
(3)由Ⅲ可得出的结论为: 。
(4)步骤Ⅳ所得蓝色溶液中阳离子为 。
(5)原混合物中各成分的质量之比是 。(不必化简)
A、B、C、D是元素周期表前三周期中的4种元素,A能与D组成AD2型化合物,AD2中核外电子总数是30,D-的核外电子排布与Al3+相同;B和C可以形成BC型化合物,BC分子中质子总数是18,BC水溶液是一种强酸,试回答:
(1)写出上述四种元素的名称:A__________,B__________,C__________,D__________。
(2)用电子式表示AD2:___________________________________ _____________________________________。
(3)D单质与水反应的化学方程式为_________________________ __________________________________________。
离子化合物AB2的阴、阳离子的电子层结构相同,1 mol AB2中含54 mol电子,且有下列反应:
①H2+B2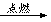 C
C
②B2+X→Y+AB2+H2O
③Y+C→AB2+Z,Z有漂白作用。
根据上述条件回答下列问题:
(1)写出下列物质的化学式:AB2__________,X________,Y________,Z________。
(2)用电子式表示AB2的形成过程:_____________________________________________。
(3)写出反应②的化学方程式:______________________________________。
A、B、C、D 4种元素,A元素所处的周期数、主族序数、原子序数均相等;B的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层少2个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C。
(1)B元素的名称为__________;B在周期表中的位置是第________周期第________族。
(2)A、B形成的化合物的电子式为________。
(3)C的元素符号为________,C的最高价氧化物的化学式为____________。
(4)D的最高价氧化物对应的水化物的化学式为________。
X、Y、Z、W是原子序数依次增大的短周期元素,且互不同族;其中只有两种为金属;X原子的最外层电子数与次外层电子数相等;X与W、Y与Z这两对原子的最外层电子数之和均为9;单质Y和W都可与浓的NaOH溶液反应。请回答下列问题:
(1)Y、Z、W的原子半径由小到大的顺序是________(用元素符号表示)。
(2)ZW2的分子式为________________。
(3)工业生产单质Y的原理是__________________(用化学方程式表示)。
(4)X与Y化学性质相似,则X与浓的NaOH溶液反应的化学方程式是___________________________________________________。
(5)0.1 mol的单质W与50 mL 1.5 mol·L-1的FeBr2溶液反应,则被氧化的Fe2+和Br-的物质的量之比是______。
下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质)。
(1)把与下面元素有关性质相符的曲线标号填入相应的空格中: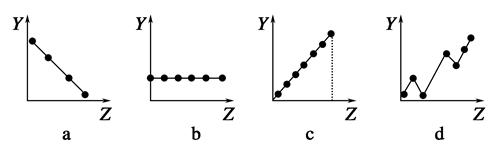
①第ⅡA族元素的价电子数________。
②第三周期元素的最高化合价________。
③F-、Na+、Mg2+、Al3+的离子半径________。
(2)元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3∶4;M元素原子的最外层电子数与电子层数之比为4∶3;N-、Z+、X+的半径逐渐减小;化合物XN常温下为气体。据此回答:
①X为________(名称),Y为________(元素符号),Z原子结构示意图为________。
②N的最高价氧化物的水化物的化学式为__________。
③工业上制取单质M的化学方程式为______________。