已知丙酮(C3H6O)通常是无色液体,易溶于水,密度小于1 g·mL-1,沸点约为55℃。要从水与丙酮的混合物中将丙酮分离出来,下列方法中最为合理的是( )
| A.蒸馏 | B.分液 | C.过滤 | D.蒸发 |
常温,下列各组离子在指定溶液中能大量共存的是
| A.pH=1的溶液中:I-、NO3-、SO42-、Na+ |
| B.由水电离的c(H+)=1×10-14mol/L的溶液中:Ca2+、K+、Cl-、HCO3- |
| C.c(H+)/c(OH-)=1012的溶液中:NH4+、Al3+、NO3-、Cl- |
| D.c(Fe3+)=0.1mol/L的溶液中:K+、ClO-、SO42-、SCN- |
、下列图示与对应的叙述相符的是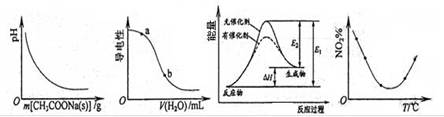
| A.图甲表示向CH3COOH溶液中逐步加入CH3COONa固体后,溶液pH的变化 |
| B.图乙表示向CH3COOH溶液中加水时溶液的导电性变化,则CH3COOH溶液的pH:a>b |
| C.图丙表示催化剂能改变化学反应的焓变 |
D.图丁表示等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应: ,相同时间后测得NO2含量的曲线,则该反应的△H<0 ,相同时间后测得NO2含量的曲线,则该反应的△H<0 |
如图是关于反应2A2(g)+3B2(g) 2C(g) △H<0的平衡移动图像,影响平衡移动的原因可能是
2C(g) △H<0的平衡移动图像,影响平衡移动的原因可能是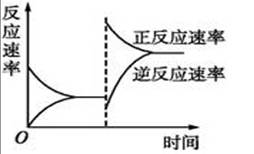
| A.升高温度,同时加压 |
| B.降低温度,同时减压 |
| C.增大反应物浓度,同时减小生成物浓度 |
| D.增大反应物浓度,同时使用催化剂 |
某温度时,浓度都是1mol/L的两种气体X2和Y2,在密闭容器中发生可逆反应生成气体Z,充分反应后X2的浓度为0.4mol/L,Y2的浓度为0.8mol/L,生成的Z的浓度为0.4mol/L,则该反应的化学方程式(Z用X、Y表示)是
A.X2+2Y2 2XY2 2XY2 |
B.2X2+Y2 2X2Y 2X2Y |
C.X2+3Y2 2XY3 2XY3 |
D.3X2+Y2 2X3Y 2X3Y |
下列关于化学反应的描述中正确的是
| A.需要加热才能发生的反应一定是吸热反应 |
| B.已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) △H=-57.3kJ/mol,则含40.0gNaOH的稀溶液与醋酸完全中和,放出57.3kJ的热量 |
| C.CO(g)的燃烧热是283.0kJ/mol,则表示CO(g)的燃烧热的热方程式为2CO(g)+O2(g)=2CO2(g) △H=-283.0kJ/mol |
| D.已知2C(s)+2O2(g)=2CO2(g) △H=akJ/mol,2C(s)+O2(g)="2CO(g)" △H=bkJ/mol,则b>a |