短周期元素W、X、Y、Z的原子序数依次增大,其中W的阴离子的核外电子数与X、Y、Z原子的核外内层电子数相同。X的一种核素在考古时常用来鉴定一些文物的年代,工业上采用液态空气分馏方法来生产Y的单质,而Z不能形成双原子分子。根据以上叙述,下列说中一定正确的是
| A.上述四种元素的原子半径大小为W<X<Y<Z |
| B.W与Y可形成既含极性共价键又含非极性共价键的化合物 |
| C.W、X、Y、Z原子的核外最外层电子数的总和为20 |
| D.有W与X组成的化合物的沸点总低于由W与Y组成的化合物的沸点 |
25℃时不断将水滴入0.1mol/L的氨水中,下列图像变化合理的是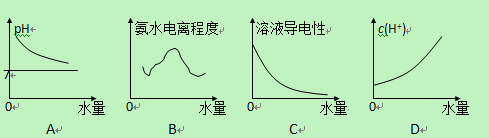
一种新型燃料电池,一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-。下列对该燃料电池说法正确的是
| A.在熔融电解质中,O2-由负极移向正极 |
| B.通入丁烷的一极是负极,电极反应为:2C4H10+52e-+26O2-=8CO2+10H2O |
| C.通入空气的一极是负极,电极反应为:O2+4e-=2O2- |
| D.电池的总反应是:2C4H10+13O2® 8CO2+10H2O |
对于平衡体系:mA(气)+nB(气)  pC(气)+qD(气) △H <0,下列判断正确的是
pC(气)+qD(气) △H <0,下列判断正确的是
A.若温度不变,将容器的体积增大1倍,此时A的浓度变为原来的0.48倍, 则m+n>p+q B.若平衡时,A、B的转化率相等,说明反应开始时A、B的物质的量之比为m:n C.若平衡体系共有气体a mol,再向其中加入b molB物质,当重新达到平衡时,气体的物质的量等于(a+b)mol , 则m+n=q+p
D.温度不变时,若压强增大为原来的2倍,达到新平衡时,总体积一定比原体积的1/2
要小
在一个固定体积的密闭容器中,加入2molA和1molB发生以下反应:2A(g)+B(g)  3C(g)+D(g),达到平衡时C的浓度为W moll/L。若维持容器体积和温度不变,按下列四种配比作为起始物质,达到平衡时,D的浓度为W/3 moll/L的是
3C(g)+D(g),达到平衡时C的浓度为W moll/L。若维持容器体积和温度不变,按下列四种配比作为起始物质,达到平衡时,D的浓度为W/3 moll/L的是
| A.3molC+1molD |
| B.2molA+2mol C |
| C.2molA+1moB+0.5molD |
| D.1molA+0.5molB+1.5molC+0.5molD |
对于可逆反应:2A(g)+B(g)  2C(g); △H<0,下列各图正确的是
2C(g); △H<0,下列各图正确的是