下列变化,需要加入适当的氧化剂才能完成的是
| A.PCl3→PCl5 | B.MnO4- →Mn2+ |
| C.SO2→SO32- | D.Cl2→HClO |
关于氢键,下列说法正确的是()
| A.分子间形成的氢键使物质的熔点和沸点升高; |
| B.冰中存在氢键,水中不存在氢键; |
| C.每一个水分子内含有两个氢键; |
| D.H2O是一种非常稳定的化合物,这是由于氢键所致 |
下列大小关系正确的是()
| A.熔点:NaI>NaBr | B.硬度:MgO>CaO |
| C.晶格能:NaCl<NaBr | D.熔沸点:CO2>NaCl |
氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,被广泛应用于电子工业、陶瓷工业等领域。在一定条件下,氮化铝可通过如下反应合成:
Al2O3 + N2 + 3 C 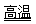 2 AlN + 3 CO 下列叙述正确的是 ( )
2 AlN + 3 CO 下列叙述正确的是 ( )
| A.在氮化铝的合成反应中,N2是还原剂,Al2O3是氧化剂 |
| B.上述反应中每生成2 mol AlN,N2得到3 mol电子 |
| C.氮化铝中氮元素的化合价为-3 |
| D.氮化铝晶体属于分子晶体 |
下列分子含有的电子数目与HF相同,且只有两个极性共价键的是()
| A.CO2 | B.N2O | C.H2O | D.CH4 |
下列关于晶体的说法一定正确的是()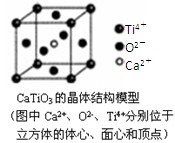
| A.分子晶体中都存在共价键 |
| B.CaTiO3晶体中每个Ti4+和12个O2-相紧邻 |
| C.SiO2晶体中每个硅原子与两个氧原子以共价键相结合 |
| D.金属晶体的熔点都比分子晶体的熔点高 |