用一种试剂除去下列物质中的杂质(括号中为杂质),写出所用试剂及离子方程式。
(1)Na2SO4溶液(CuSO4)
除杂试剂: ,离子方程式: 。
(2)FeCl2溶液(CuCl2)
除杂试剂: ,离子方程式: 。
(3)Fe(Al)
除杂试剂: ,离子方程式: 。
(1)给下列物质命名或写出结构简式:
(2)葡萄糖的结构简式
(3)乙酸与CH3CH218OH发生酯化反应的化学方程式,并注明反应条件
填写下列空白:
(1)写出表示含有8个质子、10个中子的原子的化学符号:;
(2)周期表中最活泼的非金属元素位于第族;
(3)所含元素种类是8种的周期是第、周期。
(4)氯元素在周期表中位于第周期第族。氯的最高价氧化物的化学式为,最高价氧化物的水化物的化学式为__________。
(5)物质在下列变化过程中克服的是:①共价键 ②离子键。(填序号)
HCl溶于水电解熔融NaCl制Na
电解水分解生成O2和H2
(6)在下述反应中,属于取代反应的是;属于氧化反应的是;属于加成反应的是。
①乙烯使溴水褪色 ②乙烯使酸性高锰酸钾溶液褪色③苯与浓硝酸制硝基
(10分) A、B、C、D四种元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E,D的L层电子数等于K、M两个电子层上的电子数之和。
A、B、C、D四种元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E,D的L层电子数等于K、M两个电子层上的电子数之和。 (1)A为,B为,C为。D的最高价氧化物的水化物是。
(1)A为,B为,C为。D的最高价氧化物的水化物是。 (2)写出A、B的化合物与E反应的化学方程式:
(2)写出A、B的化合物与E反应的化学方程式:
 (3)A、B两元素形成化合物属(“离子”或“共价”)化合物。
(3)A、B两元素形成化合物属(“离子”或“共价”)化合物。 (4)写出D的最高价氧化物的水化物和A反应的化学方程式:
(4)写出D的最高价氧化物的水化物和A反应的化学方程式:
(14分)
 下表是元素周期表的一部分,请回答有关问题:
下表是元素周期表的一部分,请回答有关问题:
主族 周期 周期 |
IA |
IIA |
IIIA |
IVA |
VA |
VIA |
VIIA |
0 |
| 2 |
① |
② |
③ |
|||||
| 3 |
⑤ |
⑥ |
⑦ |
⑧ |
||||
| 4 |
⑨ |
④ |
⑩ |
 (1)表中化学性质最不活泼的元素,其原子结构示意图为。
(1)表中化学性质最不活泼的元素,其原子结构示意图为。 (2)表中能形成两性氢氧化物的元素是(用元素符号表示),写出该元素的
(2)表中能形成两性氢氧化物的元素是(用元素符号表示),写出该元素的 质与⑨最高价氧化物的水化物反应的化学方程式
质与⑨最高价氧化物的水化物反应的化学方程式 (3)④元素与⑦元素形成化合物的电子式
(3)④元素与⑦元素形成化合物的电子式 (4)①、②、⑥、⑦四种元素的最高价氧化物的水化物中酸性最强的是
(4)①、②、⑥、⑦四种元素的最高价氧化物的水化物中酸性最强的是 (填化学式)。
(填化学式)。 (5)③元素与⑩元素两者核电荷数之差是。
(5)③元素与⑩元素两者核电荷数之差是。 (6)设计实验方案:比较⑦与⑩单质氧化性的强弱,请将方案填入下表。
(6)设计实验方案:比较⑦与⑩单质氧化性的强弱,请将方案填入下表。


| 实验步骤 |
实验现象与结论 |
      |
(9分)
 某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象如下表:(1)请从下表中实验现象(Ⅱ)(填A、B、C……)中选出与方案(I)(填1、2、3……)对应的实验现象,填入答案(Ⅲ)中。
某同学做同周期元素性质递变规律实验时,自己设计了一套实验方案,并记录了有关实验现象如下表:(1)请从下表中实验现象(Ⅱ)(填A、B、C……)中选出与方案(I)(填1、2、3……)对应的实验现象,填入答案(Ⅲ)中。

| 实验方案(I) |
实验现象(Ⅱ) |
答案(III) |
|
| 实验方案I |
实验现象II |
||
1.用砂纸擦后的镁带与沸 水反应,再向反应液中滴 水反应,再向反应液中滴 加酚酞 加酚酞 |
A浮与水面,剧烈反应,放出气体, 熔成—个小球,在水面上无定向移 熔成—个小球,在水面上无定向移 动,随之消失,溶液变红色。 动,随之消失,溶液变红色。 |
1 |
|
2.向新制的H2S饱和溶 液中滴加新制的氯水 液中滴加新制的氯水 |
B.产生大量气体,可在空气中燃 烧,溶液变成浅红色 烧,溶液变成浅红色 |
2 |
|
3.钠与滴有酚酞的冷水反应 |
C.反应不十分剧烈,产生的气体 可以在空气中燃烧 可以在空气中燃烧 |
3 |
|
4.镁带与2mol/L的盐酸 反应 反应 |
D.剧烈反应,产生的气体可以在 空气中燃烧 空气中燃烧 |
4 |
|
5铝条与2mol/L的盐酸 反应 反应 |
E.生成白色絮状沉淀,继而沉淀 消失 消失 |
5 |
|
6.向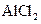 溶液中滴加 溶液中滴加 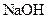 溶液至过量 溶液至过量 |
F.生成淡黄色沉淀 |
6 |
(2)通过以上实验分析了同周期元素的符号,从实验结果可以得出的结论是。