小科同学将一片土豆放入过氧化氢溶液中,发现过氧化氢溶液的分解速度加快。查阅资料后她知道土豆中含有过氧化氢酶,这是一种生物催化剂。于是她设计了如下实验:常温下将几片土豆放入甲注射器,分别往甲、乙两注射器内注入相同体积与溶质质量分数的过氧化氢溶液(如同所示),密封后观察注射器内气泡产生的速率。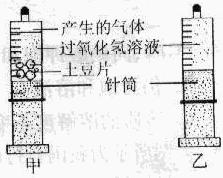
(1)小科设计的乙装置起 作用。
(2)小科把甲注射器放在0℃的环境中,发现产生气体的速率减小,说明过氧化氢酶的催化效率与 有关。
二氧化硫是形成酸雨的罪魁祸首之一。化学小组的同学想对二氧化硫进行研究,依据化学方程式Zn+2H2SO4(浓) ZnSO4+SO2↑+2H2O计算后。取一定量的锌粉与98%的浓硫酸恰好完全反应。
ZnSO4+SO2↑+2H2O计算后。取一定量的锌粉与98%的浓硫酸恰好完全反应。
提出问题:对于制得的气体,有同学认为可能含有杂质。
猜想与假设:化学小组制得的SO2中混有的杂质主要是H2。产生这一结果的主要原因是(用化学方程式和必要的文字说明)。
查阅资料:(1)CO2能与水、反应,SO2与CO2一样,也能。
(2)H2与CO一样,能将金属氧化物冶炼成金属。
(3)CaSO3难溶于水
实验验证:为证实相关分析,化学小组的同学设计了下图所示装置进行实验。 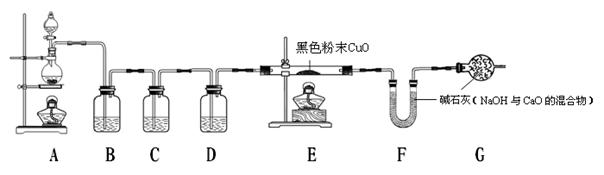
(1)B装置的作用是。
(2)混合气体中含有氢气,则E装置中观察到的现象是,反应的化学方程式为。
实验反思:小芳认为,利用上述装置可以测定混合气体中二氧化硫和氢气的质量比,要达到这一目的,实验小组必须测定下列数据中的(填字母)。
| A.参加反应的锌的质量 | B.装置B的质量增量 |
| C.氧化铜的质量 | D.装置 F的质量增量 |
红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如下图所示。
同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究。
【提出问题】久置固体的成分是什么?
【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁。
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3。
【实验探究】
甲同学的方案:
| 实验操作 |
实验现象 |
实验结论 |
| 取少量固体放于试管中,滴加足量的。 |
固体逐渐消失,有大量无色气体产生,得到浅绿色溶液。 |
固体中一定含有, 一定不含Fe2O3。 |
乙同学认为甲同学的实验并不能得出一定不含Fe2O3的结论,理由是。并设计如下实验方案继续验证。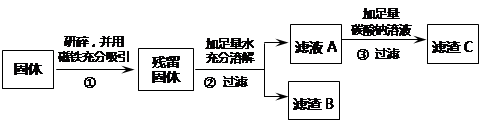
(1)②中固体溶解时放出大量热,由此可以判断固体中一定含有。
(2)③中反应的化学方程式是。
乙同学对滤渣B又进行探究。
| 实验操作 |
实验现象 |
实验结论 |
| 固体中一定含有CaCO3 和Fe2O3。 |
【反思与评价】
丙同学认为乙同学的方案中仍有一种物质不能确定。丙同学经过实验测得上述残留固体中含钙物质的总质量为1.6 g,滤渣B中CaCO3的质量为1.0 g,滤渣C的质量为1.0 g。
【实验结论】综合上述实验及所给数据,久置固体的成分是。
某小组同学用下图所示的装置进行了两组兴趣实验(a、b管的体积相等,夹持装置已略去)。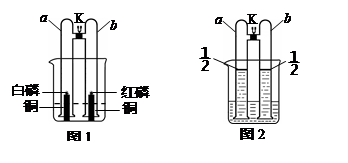
【资料】(1)白磷的着火点为40℃,红磷的着火点为240℃
(2)2NaOH + MgCl2 = Mg(OH)2↓ + 2NaCl
(1)如图1所示进行实验。关闭K,向烧杯中注入一定量的90℃的热水至图中虚线处。一段时间后,观察到a管中的现象是。其中发生反应的化学方程式是。对比a、b管中的实验现象,可得出燃烧的条件是。
(2)如图2所示进行实验。关闭K,分别用排水集气法收集体积的氢气于两管中。再将镁条和大理石分别置于a、b管口内,向烧杯内逐滴加入浓盐酸,a、b管内均有气泡产生,其中a管反应的化学方程式是。待两管内液体恰好全部排出后,向烧杯中加入过量的浓氢氧化钠溶液,溶液变浑浊。一段时间后,打开K,此时观察到a、b管中的现象是。
某研究性学习小组设计并进行了如下实验。
(1)甲组同学用下图装置制取干燥纯净的二氧化碳气体。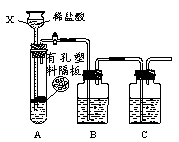
请回答下列问题:
①仪器X的名称是 ;有孔塑料隔板上的固体物质为 (填名称)。
②实验前,关闭活塞,向X中加入水使X中液面高于试管中的液面,一段时间后液面保持不变说明 。
③为除去CO2中混有的HCl气体,B装置中盛放饱和NaHCO3溶液,写出该反应的化学方程式: 。要得到干燥的CO2,C装置应盛放 (填“试剂名称”)。
④装置B、C中所装试剂的顺序不可以颠倒,理由是: 。
(2)乙组同学围绕C还原CuO产生的红色固体是否一定是Cu进行探究。
【查阅资料】 ①在空气中高温灼烧时,CuO会分解生成Cu2O;Cu2O粉末呈红色,在高温下性质稳定;②Cu2O在酸性溶液中不稳定,如在稀硫酸中:Cu2O+H2SO4=CuSO4+Cu+ H2O。
【提出猜想】猜想Ⅰ:红色固体是Cu;猜想Ⅱ:红色固体是Cu2O;猜想Ⅲ:红色固体是 。
【实验探究】同学们又分为两组,分别进行以下实验:
①第一组同学取一定质量的红色固体a g ,在空气中高温灼烧,直到质量不再发生改变,称量所得固体质量为b g 。并进行数据分析:若a = b,则猜想成立;若b>a,则说明红色固体中一定含有物质。
②第二组同学没有用测量质量的方法也得出了红色固体中含有Cu2O的结论。该同学设计的实验方法是。(写出“实验操作、现象和结论”)
【解释与结论】 根据实验探究,可知C还原CuO时除了发生2CuO+C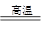 2Cu +CO2↑的反应外,还可能发生的化学反应方程式:。
2Cu +CO2↑的反应外,还可能发生的化学反应方程式:。
【拓展延伸】同学们又就Cu2O是否具有氧化性展开了讨论,请你设计实验方案:。
【实验反思】通过以上实验探究,你对“问题的发现与解决”有何认识?。
几位同学理化生实验考试中做了氢氧化钠和稀盐酸的实验,考完后对两者反应后溶液中的溶质的组成进行了进一步的探究。甲同学猜想溶液中只含有氯化钠;乙同学猜想可能含有氯化钠、氢氧化钠和稀盐酸。
①两位同学中有位同学的猜想是不正确的,请你帮他分析原因。②你再提出一个正确的猜想,并设计实验验证你的猜想。