小红同学为了探究二氧化碳与水反应的生成物,做了如下实验:向盛有石蕊试液的试管中通入二氧化碳,观察到紫色石蕊试液变成红色,为了探究是什么物质使紫色石蕊试液变红了,小红同学作了大胆猜想,并用石蕊试液染成紫色的干燥小花设计了下列四个实验方案来验证自己的猜想(如下图)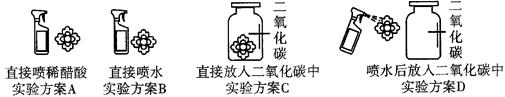
(1)请和小红仪器来完成下表:
| 猜想 |
实验方案 |
实验现象 |
结论 |
| 可能是CO2使石蕊变红 |
C |
小花不变色 |
|
| |
B |
小花不变色 |
猜想错误 |
| 可能是CO2和水发生反应的生成物使石蕊变红 |
|
|
猜想正确 |
(2)小红同学做了一个对比实验来确定CO2于水反应生成具有酸性的物质,此对比实验方案是 (填上图中的实验方案序号),生成该酸的化学方程式为 。
为提高实验探究能力,某化学兴趣小组的同学在老师的指导下,对一瓶久置出现变质硬化的氢氧化钙固体进行如下探究活动。
【探究活动一】试验硬化的氢氧化钙样品是否完全变质
(1)用化学方程式表示氢氧化钙变质的原因:。
(2)检验氢氧化钙样品是否完全变质,进行如下实验:
| 实验步骤 |
实验现象 |
实验结论 |
| 取氢氧化钙样品少量,研细后加适量蒸馏水充分混合后静置, | 该样品还含有氢氧化钙 |
【探究活动二】测定样品中含有的变质固体(以下用
表示)的质量分数
取3克部分变质的氢氧化钙样品与足量的稀盐酸反应,测量生成气体的体积(气体不溶于植物油),从而计算出样品中R的质量,便可求出样品中
的质量分数。实验装置(气密性良好)如图1所示。
(3)将稀盐酸滴入样品中,产生气体的化学方程式为,反应一段时间后,当观察到(填实验现象),才停止滴加稀盐酸。
(4)实验中量筒的作用是。
(5)实验结束后,量筒内进入水的体积如图2所示,其读数为
。已知在该实验条件下,生成气体的密度为2
,通过计算,样品中
的质量分数为。
(6)上述图1所示实验装置和相关试剂,用来实验测定样品中
的质量分数是比较粗略的,请简要说明测定数据存在误差的原因:(写一个)。
阅读下面科普短文(原文作者:段翰英等)。
我国制作泡菜的历史悠久。制作泡菜是把新鲜蔬菜泡在低浓度的盐水里,经发酵而成。泡菜品种繁多、风味独特、口感鲜脆。
蔬菜中含有硝酸盐。硝酸盐对人体无直接危害,但转化成亚硝酸盐后,就会产生危害。亚硝酸盐[如亚硝酸钠(
)]与胃酸(主要成分是盐酸)反应,产生亚硝酸(
)和氯化物(如
)。亚硝酸不稳定,产生的二氧化氮进入血液与血红蛋白结合,导致中毒。
泡菜中含亚硝酸盐吗?含量有多少?含量受什么因素影响呢?
经实验测定发现,食盐水浓度和泡制时间对泡菜中亚硝酸盐含量有一定影响。下图为室温下,食盐水浓度和泡制时间与芹菜泡制过程中亚硝酸盐含量的关系。
用不同的蔬菜进行测定,变化趋势与芹菜相似。
实验表明,发酵温度对泡菜中亚硝酸盐的生成量及生成时间也具有明显的影响。泡菜发酵过程中,泡制温度较高时,亚硝酸盐含量最大值出现的早,且数值低。这与温度较高有利于乳酸菌的繁殖有关。
实验还表明,泡制过程中添加姜汁和维生素
,都能有效地减少亚硝酸盐的生成。
现代医学证明,泡菜中的乳酸和乳酸菌对人体健康有益,具有抑制肠道中的腐败菌生长、降低胆固醇等保健作用。但是,有些泡菜盐分或糖分过高,对高血压和糖尿病等慢性病患者不利。另外,泡制过程也会造成某些营养素的流失。(有删改)
依据文章内容,回答下列问题。
(1)泡菜中的亚硝酸盐是由转化成生的。
(2)亚硝酸钠能与盐酸反应,该反应属于基本反应类型中的反应。
(3)室温下,用芹菜制作的泡菜,最佳食用时间是填字母序号,下同)。
A.泡制2-3天B.泡制5-6天C.泡制12天后
(4)下列关于制作泡菜的说法中,合理的是。
A.最好加入一些姜汁
B.最好在较低温度下泡制
C.最好加入一些富含维生素
的水果
D.最佳食用期的泡菜中亚硝酸盐的含量与泡制时的食盐水浓度无关
(5)请你为喜欢吃泡菜的人提一条食用泡菜的建议:。
众所周知,酚酞溶液遇
溶液变红。但是,在分组实验中(如图所示),出现了意想不到的现象:有的溶液变红后褪色;有的出现白色浑浊物。
【提出问题】分组实验中,出现意想不到的现象的原因是什么呢?
【查阅资料】酚酞溶液由酚酞固体溶于酒精配制而成。
【猜想与假设】
Ⅰ.红色褪去,与
溶液和空气中的
反应有关。
Ⅱ.红色褪去,与
溶液的浓度有关。
Ⅲ.出现白色浑浊物,与酚酞溶液的浓度有关。
【进行实验】
| 实验 |
实验操作 |
实验现象 |
|
| 1 |
向盛有2 mL =
溶液的试管中滴加5滴0.5%的酚酞溶液 |
溶液变红 |
|
| 2 |
 |
1号试管0.1min红色褪去 2号试管5min红色褪去 3号试管30min红色明显变浅 4号试管120min红色无明显变化 |
|
| 3 |
取3支试管,分别加入2 mL水,…… |
酚酞溶液浓度/% |
浑浊程度 |
| 5 |
大量浑浊物 |
||
| 2 |
少量浑浊物 |
||
| 0.5 | 无浑浊物 |
【解释与结论】
(1)
与
反应的化学方程式为。
(2)实验1的现象表明,猜想与假设1(填"成立"或"不成立")。
(3)由实验2得出结论:出现"溶液变红后褪色"现象的原因是。
(4)实验3的操作步骤:取3支试管,分别加入2ml水,。
【反思与评价】
(5)依据现有实验,为了确保红色不变,若酚酞溶液浓度为0.5%,建议选用
溶液的浓度为%。
(6)有同学认为,仅通过实验3得出"猜想与假设Ⅲ成立"证据不足,理由是。
已知
通入澄清石灰水中,溶液变浑浊,继续通
气体由浑浊又变澄清,
,由此某化学兴趣小组欲探究
与
溶液反应后的溶质组成。
【提出问题】
与
溶液反应后的溶质组成
【查阅资料】1、
2、盐酸滴入碳酸钠溶液中,实际反应分两步进行
第一步反应:
第二步反应:
【提出猜想】猜想1:溶质为
猜想2:溶质为(填化学式,以下同)
猜想3:溶质为
猜想4:溶质为
【实验方案】I甲组同学为确定
与
溶液反应后所得溶液中溶质组成,设计如下实验方案。
(1)向所得溶液中加入足量的
溶液,若有白色沉淀生成,过滤后向溶液中加入足量的稀盐酸无气泡产生,则溶质为。
(2)向所得溶液中加入足量的
溶液,若无白色沉淀生成,溶液中加入足量的稀盐酸有气泡产生,则溶质为。
(3)向所得溶液中加入足量的
溶液,若有白色沉淀生成,过滤后向溶液中加入足量的稀盐酸有气泡产生,则溶质为。
II乙组同学根据甲组同学的猜想,通过定量分析绘制出向所得溶液中逐滴加入稀盐酸的质量与生成二氧化碳的质量关系示意图,请根据图像确定溶质成分。
某化学活动小组在一次实验中进行了如图所示实验:
此时观察到的实验现象是(1)__________________________。
实验后,小组同学充分振荡U形玻璃管,将U形玻璃管内的物质过滤后,对滤液成分产生了浓厚的兴趣,进行了进一步的探究活动。
【提出问题】滤液中除Na+外,还含有什么离子?
【猜想与假设】A同学:含有OH-、Cl-、C032-
B同学:含有OH-、Cl-、Ba2+
C同学:含有(2)__________________(填离子符号)
【实验探究】B同学为了验证自己的猜想,取滤液于试管中,向其中滴加少量的硫酸钠溶液,观察到无明显现象。由此B同学得出结论:自己的猜想不成立,A同学的猜想成立。
【评价与交流】请你评价B同学的结论:(3)______________________。同学们经过讨论后一致认为:B同学在验证自己的猜想时,若将所加试剂调换成足量的另一种试剂(4)_____________(填化学式),既能验证自己的猜想.也能确定滤液中的离子成分。
C同学取该试剂进行实验,最终确定了滤渡中的离子成分。
【归纳与总结】通过上述实验我们能够总结出:在确定化学反应后所得溶液中的离子成分时,一般应加入(5)___________________,验证(6)____________________________就可以确定溶液中的离子成分。