已知反应:2HBr(g)  Br2(g)+H2(g),在四种不同的条件下进行,Br2、H2起始的浓度为0,反应物HBr的浓度(mol/L)随反应时间(min)的变化情况如下表:
Br2(g)+H2(g),在四种不同的条件下进行,Br2、H2起始的浓度为0,反应物HBr的浓度(mol/L)随反应时间(min)的变化情况如下表:
| 实验序号 |
实验温度 |
0 |
10 |
20 |
30 |
40 |
50 |
60 |
| 1 |
800℃ |
1.0 |
0.80 |
0.67 |
0.57 |
0.50 |
0.50 |
0.50 |
| 2 |
800℃ |
C2 |
0.60 |
0.50 |
0.50 |
0.50 |
0.50 |
0.50 |
| 3 |
800℃ |
C3 |
0.92 |
0.75 |
0.63 |
0.60 |
0.60 |
0.60 |
| 4 |
820℃ |
1.0 |
0.40 |
0.25 |
0.20 |
0.20 |
0.20 |
0.20 |
下列说法正确的是( )
A.从上表数据分析,2HBr(g)  Br2(g)+H2(g)正反应为放热反应
Br2(g)+H2(g)正反应为放热反应
B.实验2中HBr的初始浓度C2=1.0 mol/L
C.实验3反应速率小于实验1的反应速率
D.实验4一定使用了催化剂
X、Y、Z是周期表中相邻的三种短周期元素,它们原子半径依次减小,X与Z的核电荷数之比为3∶4,X、Y、Z分别与氢元素形成氢化物。下列叙述正确的是
| A.Z是第二周期IVA族元素 |
| B.最高价氧化物对应的水化物的酸性: Y﹥X |
| C.非金属性:X﹥Y﹥Z |
| D.X、Y、Z的氢化物稳定性逐渐减弱 |
关于化学键的叙述中,正确的是
| A.离子化合物可能含共价键 | B.共价化合物可能含离子键 |
| C.离子化合物中只含离子键 | D.离子化合物中一定含有金属离子 |
下图是可逆反应A2 + 3B2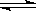 2C2在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是
2C2在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是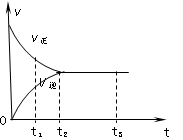
| A.t1时,只有正方向反应 | B.t2时,反应未到达最大限度 |
| C.t2- t3,反应不再发生 | D.t2- t3,各物质的浓度不再发生变化 |
在一定条件下,对于密闭容器中进行的反应:N2 (g) + 3H2 (g) 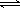 2NH3 (g),下列说法能充分说明该反应已经达到化学平衡状态的是
2NH3 (g),下列说法能充分说明该反应已经达到化学平衡状态的是
| A.正、逆反应速率都等于零 | B.N2、H2、NH3的浓度均不再变化 |
| C.N2、H2、NH3在容器中共存 | D.N2、H2、NH3的浓度相等 |
下图为番茄电池,下列说法正确的是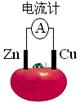
| A.一段时间后,锌片质量会变小 | B.铜电极附近会出现蓝色 |
| C.电子由铜通过导线流向锌 | D.锌电极是该电池的正极 |