自然界的水含有各种杂质,可以用不同的方法进行净化。
(1) 下图所示是用空塑料饮料瓶、带导管的单孔胶塞、蓬松棉、纱布、活性炭、小卵石、石英沙等材料自制的一个简易净水器。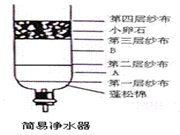
①根据上述净化材料的特性,B层放置的材料最好是______;
②该净水器不同位置的纱布所起的主要作用不同,其中第二层纱布的主要作用是___;
③你认为上述简易净水器(填“可以”或“不可以”)_____将硬水变成软水。检验一份自来水样是硬水还是软水,方法是向水样加入_______来鉴别,生活中将硬水变成软水的方法是________。
(2) 实验室为了配制溶液;常用如右图所示的装置制取净化程度较高的蒸馏水。
① 在连接好装置后,应先进行_____的操作,再加入水和沸石进行蒸馏;
② 在烧瓶中加入沸石的目的是_______。
⑶ 节约用水是每个公民的义务,下列用水方式应该提倡的是______(填字母序号)。
a.用漱口杯接水刷牙
b.不间断地边流水边洗衣
c.用淘米水、洗菜水浇花、冲厕所
d.用喷灌、滴灌的方法浇灌农田和园林
氯化钠溶液中含有杂质CaCl2、MgCl2和Na2SO4,依次通过以下操作将其除去:①加入过量的氢氧化钠溶液,②加入过量的氯化钡溶液,③加入过量的碳酸钠溶液,④过滤,⑤加入适量的盐酸至溶液呈中性。
(1)操作②和操作③的顺序能否颠倒?为什么?____________________
(2)操作④过滤后溶液中的溶质有哪些?____________________
呼吸面具中的“氧气再生剂”的主要成分是淡黄色固体过氧化钠(Na2O2),它在空气中易与水或二氧化碳发生化学反应而变质。已知过氧化钠与水反应的化学方程式为:2Na2O2+2H2O=4NaOH+O2↑;过氧化钠与二氧化碳反应生成一种碳酸盐和氧气。
(1)诸写出过氧化钠与二氧化碳反应的化学方程式____________________。
(2)向变质后的过氧化钠固体中加入足量水,请你设计实验,验证该水溶液中含有的两种溶质。(简要写出实验步骤及现象)____________________
化学在“节能减排”中发挥着重要作用。
(1)液化天然气是我市正在推广的公交车燃料,它具有燃烧效率高、污染小的优点。请写出天然气完全燃烧的化学方程式____________________。
(2)氢化镁(MgH2)固体可为氢动力汽车提供能源,其与水反应生成氢氧化镁和氢气。写出该反应的化学方程式____________________。
(3)氢能源被称为“21世纪最理想的能源”,它除了具备原料来源广、燃烧热值高的优点外,还有什么优点?____________________
(4)为节约能源,使燃料充分燃烧,应考虑的因素是什么?____________________(写出一条即可)
有CO、CO2和N2的混合气体40 g,其中碳元素的质量分数为30%,使该混合气体与足量灼热的氧化铁完全反应,再将气体通入过量的澄清石灰水中,写出以上过程中发生反应的两个化学方程式:________________________;________________________。充分反应后得到白色沉淀的质量为___________________________。
请结合下图回答问题;
(1)实验室可用A装置制取CO2,其化学方程式为__________________,若将A改为B,其优点是________________________。
(2)为了得到纯净、干燥的CO2,除杂装置导管的正确连接顺序是____(填字母)。
| A.1—2—4—3 | B.2—1—3—4 |
| C.4—3—1—2 | D.3—4—2—1 |