为了探究质量守恒定律,某同学设计了右图“白磷燃烧前后质量测定”的实验,请分析有关问题:
(1)装置:锥形瓶的底部铺有一层细沙,其作用是 ____________________________
(2)实验现象:白磷燃烧产生________________,气球先变大又变小。气球先变大后又变小的原因____________________________
(3)燃烧后称量:发现托盘天平指针偏向右边,造成的原因可能是_________________。
(4)反思:白磷燃烧_________(填“遵守”或“不遵守”)质量守恒定律,理由是_____________。
A图为实验示意图,在室温情况下,烧杯中盛装的是甲物质的溶液,试管①中盛装的是乙物质的溶液,试管②中盛装的是丙物质的溶液。当它们由室温升到80℃时,发现烧杯中甲物质没有明显变化,而试管①中盛装的是乙物质全部溶解,试管②中有丙物质析出。B图表示三种物质的溶解度曲线。请你据此现象回答下列有关问题: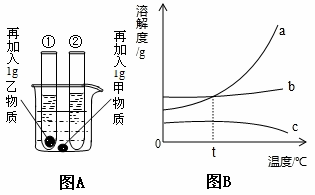
(1)室温时,(选填“烧杯”、“试管①”或“试管②”)中溶液可能是不饱和溶液;
(2)上图能表示甲物质的溶解度曲线的是(选填a、b或c);
(3)若乙物质溶液中混有少量的甲物质,提纯乙物质可采取的方法是
(4)对于甲、乙两物质饱和溶液,在温度时,乙物质的溶质质量分数一定比甲物大.
节假日或双休日,去郊游野炊实为一大快事。但野炊的过程中可能会遇到下面一些问题,你将如何处理呢?
(1)在“灶”上悬挂野炊锅时,应调节野炊锅到合适的高度.你觉得原因可能是
(2)野炊食谱如下:主食:馒头;配菜:烤火腿、鲫鱼汤、五香豆干。从营养角度来看,你可以再准备一样(填字母序号);
A.炒鸡蛋 B.牛奶 C.黄瓜 D.烤野兔肉
(3)若不小心被蚊虫叮咬(蚊虫能分泌出蚁酸),下列物质可用于涂抹以减轻疼痛的是 ()(填字母)
A.食醋(pH<7)B.食盐水(pH=7)C.肥皂水(pH>7)
钠是一种非常活泼的金属,它可以和冷水直接反应生成氢气和一种碱,但它不与煤油反应.把一小块银白色的金属钠投入盛有蒸馏水的烧杯中(如图a),可以看到钠浮在水面上,与水发生剧烈反应,反应放出的热量使钠熔成小球,甚至会使钠和生成的氢气都发生燃烧.如果在上述盛蒸馏水的烧杯中先注入一些煤油,再投入金属钠,可以看到金属钠悬浮在煤油和水的界面上(如图b),同样与水发生剧烈的反应,但是不发生燃烧.则:
(1)写出钠和水反应的化学方程式 反应类型是
(2)在第二个实验中,钠也与水发生反应,但不发生燃烧,这是因为
(3)第一个实验中,钠浮在水面上;在第二个实验中,钠悬浮在煤油和水的界面上.
这两个现象说明了金属钠具有的物理性质是
生产、生活中处处有化学。
(1)用洗洁精清洗油污,是利用了洗洁精的作用。
(2)厨房中的酸性调味剂中含有的酸是(写化学式)。
(3)长沙新奥燃气公司给用户输送的是天然气,在初次使用之前需要通入氮气,通入氮气的目的是什么?
请写出天然气燃烧的化学方程式
请结合下列实验常用装置,回答有关问题.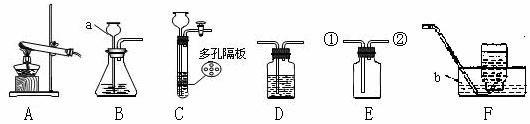
(1)仪器a的名称是。
(2)若用B、F组成制取某气体的装置,写出制取此气体的化学方程式为,
若要获得干燥的二氧化碳,除发生装置外,还应选用D装置,并在该装置中盛放试剂(填写试剂名称).如果用E装置收集该气体则气体从端进入(填“①”或“②”)。
(3)乙炔(C2H2)是无色、无味、易燃的气体,乙炔的密度比空气略小,难溶于水。乙炔(C2H2)气体和氧气反应能产生高温火焰,工人师傅常用氧炔焰切割或焊接金属。乙炔由碳化钙(块状固体)与水反应生成,同时生成一种白色固体。已知碳化钙与水反应非常剧烈。实验室欲制取并收集纯净的乙炔,要求做到节约、安全、随时发生、随时停止,你选择的装置是。