"车用乙醇汽油"的推广和使用将会缓解石油资源紧张。乙醇(化学式为C2H5OH)完全燃烧生成CO2和H2O.
(1)写出乙醇完全燃烧的化学方程式 。
(2)乙醇燃烧时如果氧气量不足,可能还有CO生成.用以下装置确证乙醇燃烧产物有CO和CO2,应将乙醇燃烧产物依次通过(按气流从左至右顺序填装置编号) 。
正确连接后的装置仍存在不足,请指出其不足之处 。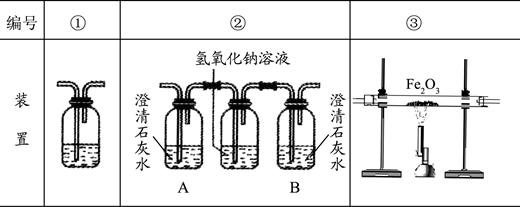
(3)装置②中A、B两瓶均盛有澄清的石灰水,其作用分别是 。
(4)写出装置①中所盛溶液名称及该溶液的作用 。
果蔬洗盐既能去除水果和蔬菜表面的农药,又能杀菌、去小虫,近几年比较流行。某品牌果蔬洗盐常温下为白色固体,小敏取用时不小心将其洒落在天然气的火焰上,发现火焰呈黄色,这引起了小敏探究其成分的兴趣。
【查阅资料】1.钠及其化合物灼烧时火焰呈黄色。
2.农药大多数呈酸性。
【提出猜想】猜想一:碳酸钠
猜想二:碳酸氢钠
猜想三:碳酸钠和碳酸氢钠的混合物
小敏做出以上猜想的依据是 。
【查阅资料】碳酸氢钠受热分解产生二氧化碳、碳酸钠和水。
【进行实验】
|
实验步骤 |
实验现象 |
分析与结论 |
|
①取一定量果蔬洗盐加热至固体质量不再改变,将生成的气体全部通入足量澄清石灰水中 |
有气体生成,澄清石灰水中产生白色沉淀 |
生成气体的化学方程式: ,该品牌果蔬洗盐中含有 |
|
②将①加热后残留固体全部溶于水,加入足量氯化钙溶液 |
产生白色沉淀 |
/ |
|
③分别测量①和②产生沉淀质量 |
①中产生沉淀2.5g,②中产生沉淀质量 |
该品牌果蔬洗盐中含有碳酸钠 |
【继续探究】
小敏想到妈妈以前常用食盐水洗水果,猜想该品牌果蔬洗盐中还可能含有氯化钠。她向其水溶液中加入 至溶液呈酸性,再加入 溶液,观察到有白色沉淀生成,证明有氯化钠。
【拓展延伸】
该品牌果蔬洗盐不可直接食用,使用后,要用清水冲洗。
同学们学习了复分解反应发生的条件后,利用所学知识对稀盐酸与如图中的三种物质之间能否发生反应作出判断,并进行实验验证:
|
组别 |
甲 |
乙 |
丙 |
|
实验示意图 |
|
|
|
|
能否反应 |
能 |
能 |
能 |
|
实验现象 |
无明显现象 |
有气泡产生 |
产生白色沉淀 |
同学们判断Ca(OH)2溶液和稀盐酸能发生化学反应的依据是生成物中有 生成。
【提出问题】
怎样证明Ca(OH)2溶液与稀盐酸发生了反应?
【分析讨论】
同学们经过讨论后认为,如果盐酸和氢氧化钙减少(或消失),或者有新物质生成,都能证明反应已经发生。
【查阅资料】
CaCl2溶液呈中性。
【实验探究】
|
方案 |
实验操作 |
实验现象 |
实验结论 |
|
方案一 |
小羽取少量Ca(OH)2溶液于试管中,先滴入2~3滴无色酚酞溶液,再加入稀盐酸 |
|
反应物消失,二者发生了反应 |
|
方案二 |
小美向甲组反应后的溶液中加入适量AgNO3溶液 |
产生白色沉淀 |
有新物质生成,二者发生了反应 |
【实验评价】
小凯认为小美的结论不正确,理由是 。
【总结归纳】
(1)Ca(OH)2溶液与稀盐酸发生了化学反应,其反应的化学方程式为 。
(2)对于无明显现象的反应,我们可以分析比较反应物和生成物的性质,从多个角度设计实验进行证明。
【拓展延伸】
将少量CO2通入NaOH溶液中也无明显现象,请你设计一个实验方案证明二者发生了反应 (写出操作方法和现象)。
在探究碱溶液的化学性质时,某兴趣小组将两支规格相同且充满二氧化碳的试管分别插入氢氧化钙溶液和氢氧化钠溶液中,摆动试管。如图所示:
【观察现象】
(1)实验A中试管内液面上升,试管内出现浑浊的现象,发生反应的化学方程式为 。
(2)实验B中试管内液面上升,无浑浊现象。
【提出问题】
氢氧化钠溶液与二氧化碳是否发生了反应。
【讨论交流】
(1)甲同学根据B试管内液面上升的现象,认为氢氧化钠溶液与二氧化碳发生了反应。
(2)乙同学认为:由此实验直接得出二氧化碳和氢氧化钠溶液能发生反应的结论还不够严密。你认为乙同学的理由是 。
(3)丙同学认为:可以从化学反应有新物质生成的角度,来证明二氧化碳和氢氧化钠溶液是否发生化学反应。他发现实验台上有下列试剂:酚酞溶液、石蕊溶液、稀盐酸、稀硫酸、氯化钙溶液、硝酸钡溶液。请你从中选择一种试剂,帮助丙同学设计实验,验证二氧化碳和氢氧化钠溶液是否发生了化学反应。
【实验验证】
|
实验步骤 |
实验现象 |
实验结论 |
|
|
|
二氧化碳与氢氧化钠溶液 化学反应(填“发生”或“不发生”) |
【拓展应用】
根据以上实验现象,参考小资料,选用“饱和氢氧化钠溶液”或“饱和氢氧化钙溶液”完成下面问题:
小资料:20℃时氢氧化钠的溶解度为109g,氢氧化钙的溶解度为0.165g。
(1)鉴别二氧化碳气体,应该选用 。
(2)吸收二氧化碳气体,应该选用 。

在学习了单质碳的化学性质后,某化学兴趣小组的同学对含碳化合物燃烧后的产物进行了探究。
【提出问题】乙醇燃烧后的产物是什么?
【查阅资料】①无水硫酸铜为白色粉末,遇水会变蓝;
②氯化钙有吸水性,可做干燥剂。
【做出猜想】猜想一:产物中含有CO、H2O;
猜想二:产物中含有CO2、H2O;
猜想三:产物中含有(1) 。
【进行实验】同学们设计了如图的实验:检查装置气密性后,将乙醇燃烧的产物依次通过如图所示的装置进行验证;(部分夹持固定装置省略;B、D、G装置中均为澄清的石灰水)

(2)装置B的作用是 。
(3)F装置中若发生反应,则化学方程式是 。
【解释与结论】经过实验,同学们认为猜想三成立。
(4)实验中能观察到的现象是① ;装置C中发生反应的化学方程式为② 。
【反思与评价】实验结束后,由于小丽同学的操作不当造成了仪器损坏,小组内同学针对这个事故,进行了分析和讨论。
(5)为了避免此事故再次发生,同学们对该装置进行了创新和改进,你认为他们的改进是 (文字说明或画图都可)。
化学兴趣小组的同学在验证硫酸的性质时,进行了以下实验。

【实验一】浓硫酸稀释过程中的能量变化。
图一实验中,观察到用石蜡固定在铜片下的乒乓球脱落,此现象说明浓硫酸溶于水 。
【实验二】溶液浓度对硫酸化学性质的影响。
图二实验中,观察到很快变黑的是滤纸 (填“A”或“B”),由此可知,硫酸溶液的浓度不同,腐蚀性不同。
【实验三】稀硫酸的化学性质。
小组同学按图三进行实验。
(1)试管1中发生反应的化学方程式为 。
(2)试管2中可观察到的现象是 。
(3)向试管3中滴加了足量的稀硫酸仍无明显现象,要证明二者已经发生反应,可选用
(填字母序号)继续进行实验,以达到实验目的。
A.酚酞溶液
B.氯化钡溶液
C.硫酸铜溶液
(4)小组同学将4、5两支试管反应后的物质倒入同一洁净的烧杯中,充分反应后过滤,得到无色滤液和白色沉淀。同学们对白色沉淀的成分产生了兴趣,继续进行实验。
【提出问题】白色沉淀的成分是什么?
【作出猜想】猜想一:
猜想二:BaSO4、BaCO3
【实验与结论】
|
实验操作 |
实验现象 |
实验结论 |
|
取少量白色沉淀与试管中,向其中加入足量的稀盐酸。 |
。 |
猜想二成立。 |
实验结束后,在老师指导下同学们对废液缸中的固体物质进行了回收。在检验废液时发现硫酸过量,为防止其污染环境,从实验成本的角度考虑,向该废液中加入适量的
(填一种具体物质),处理后再排放。