碱石灰是实验室中常用的干燥剂。
[资料]
①碱石灰是氧化钙、氢氧化钠的固体混合物,易吸收空气中二氧化碳和水蒸气。
②氯化钙溶液呈中性。
[提出问题]
对实验室中久置的碱石灰样品的成分进行探究。
[进行猜想]
久置碱石灰样品中可能含有CaO、NaOH、Ca(OH)2、Na2CO3、CaCO3中的两种或两种以上成分。上述五种物质中,属于碱的是_____________________。
样品中可能含有Ca(OH)2、Na2CO3的原因是(请用化学方程式表示)_________、_______ 。
[实验过程] 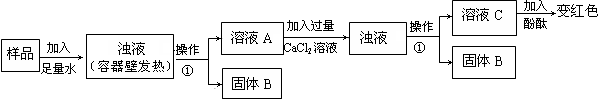
试回答下列问题:
(1)操作①的名称是_________。
(2)根据实验操作及现象,下列说法正确的是__________。
| A.样品中加水后容器壁发热,说明样品中一定含有CaO |
| B.样品加足量水后仍有固体,说明样品中一定含有CaCO3 |
| C.溶液A加入CaCl2溶液后产生固体,说明样品中一定含有Na2CO3 |
| D.溶液C加入酚酞变红,说明样品中一定含有NaOH |
(3)向溶液A中加入过量的CaCl2溶液的操作中,判断加入试剂过量的方法是___________________。
(4)写出溶液C中所含阴离子的符号____________________。
[实验结论]
该久置碱石灰样品中肯定含有的成分是(填化学式) ,其它成分尚不能确定。
在溶液中较难制得纯净的Fe(OH)2,原因是Fe(OH)2不稳定,在水中只要有一点氧气就极易反应生成红褐色沉淀Fe(OH)3。写出其反应的化学方程式:
。
用下面两种精心设计的方法可以制得白色的Fe(OH)2沉淀。
方法一:用不含氧气的蒸馏水配置FeSO4溶液与NaOH溶液,然后反应制备。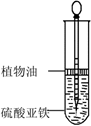
a.除去蒸馏水中溶解的氧气,常采用的方法。
b.如图所示,用长滴管吸取不含O2的NaOH溶液,插入FeSO4溶液液面下,再挤出NaOH溶液。试管中油层的作用是。
方法二:用如图装置来制备。
a在装置Ι中加入Fe和稀H2SO4,写出其反应的化学方程式;在装置Ⅱ中加入NaOH浓溶液。
b为了制得白色Fe(OH)2沉淀,需要下列步骤,其顺序为
①气密性检查 ②气体验纯
③加入试剂塞紧橡皮塞 ④打开止水夹 ⑤夹紧止水夹。
c.写出试管Ⅱ中发生的化学反应方程式
、。
这样生成的Fe(OH)2沉淀能较长时间保持白色。
铝制品却不宜长时间盛放腌制食品。资料显示:“铝制品表面虽然有一层致密的氧化膜保护……氯化钠也会破坏氧化膜的结构,加速铝制品的腐蚀。”
【提出问题】氯化钠溶液中的哪一种离子对铝制品表面的氧化膜产生了破坏作用?
【实验方案】请填写下面表格中的空格。
| 序号 |
实验1 |
实验2 |
实验3 |
| 方案 |
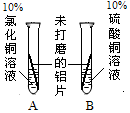 |
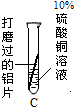 |
 |
| 现象 |
A中铝片表面有红色固体析出; B中铝片无明显现象。 |
与A中的现象相同 |
|
| 结论 |
溶液中对氧化膜产生了破坏作用的离子可能是。 |
除去表面氧化膜的铝片会与CuSO4溶液反应。该反应 的化学方程式 。 |
验证了实验1的结论。 |
【反思】针对实验3,同学认为还应增做一个对比实验,方案是向(从“A、B、C、D”中选择)试管中再加入Na2SO4溶液,结果无明显现象。该实验可证明溶液中对氧化膜不产生破坏作用的离子是。
碳酸氢钠是一种重要的盐类物质,在生活中用途广泛。小红同学设计实验对碳酸氢钠的性质进行了探究。请你参与她的探究活动。
【探究实验1】碳酸氢钠溶液的酸碱性。
【实验方案】取少量该固体加入试管中,加适量水溶解,再滴入几滴酚酞试液,振荡。现象:溶液变成浅红色。结论:①。
【探究实验2】能与酸反应。
【实验方案】取少量该固体加入试管中,滴加稀盐酸。现象:②。反应的化学方程式为:③。
【探究实验3】碳酸氢钠的热稳定性。
【实验方案】设计实验装置如图,并进行实验。
现象: 试管口有水珠出现,澄清石灰水变浑浊。充分加热后,试管中留下白色固体。
结论:碳酸氢钠受热有二氧化碳.水和白色固体生成。
请你帮小红设计实验,证明试管中留下的白色固体是Na2CO3,而不是NaOH。(所选试剂不能用酸)
步骤:④;
现象:⑤。
试写出碳酸氢钠受热发生反应的化学方程式:⑥。
【拓展应用】根据以上探究,请说出碳酸氢钠在日常生活中的一种用途⑦。
有某固体混合物,已知该混合物中可能含有FeCl3、Na2SO4、NH4NO3、CuSO4四种物质中的两种或多种。为探究其组成,做了如下实验(设过程中所有发生的反应都恰好完全反应)。
步骤①:向一定量固体混合物中加入适量NaOH溶液,加热,充分反应,过滤。发现有无色气体A生成,得到无色溶液B和蓝色沉淀C。
步骤②:向无色溶液B中加入适量BaCl2溶液,充分反应,过滤,得到溶液D和沉淀E。
试根据实验过程和发生的现象填写以下空白:
(1)用湿润的红色石蕊试纸测试气体A,试纸变__________色。
(2)固体混合物里.上述四种物质中,肯定不存在的物质是______________(写化学式)。
(3)在溶液D中,肯定存在的酸根离子是(写离子符号)_____________。
(4)步骤②中发生反应的化学方程式为______________________________________。
(5)固体混合物里,上述四种物质中,还不能确定存在的物质是(写化学式)________,
得此结论的理由是_________________________________________________________。
小亮同学对课本中C和CuO反应的产物进行了进一步的探究。以下是他进行实验的部分流程(装置气密性良好):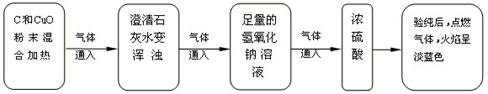
(1)通过以上实验,可知产物中有气体。
(2)取出反应后的固体,观察呈红色。
【查阅资料】
①C也能将CuO还原为红色固体Cu2O(氧化亚铜)
②Cu2O + H2SO4(稀)= Cu + CuSO4 + H2O
【猜想】(a)红色固体只是Cu;(b)_______;(c)红色固体是Cu和Cu2O的混合物
【实验】请你设计一个实验证明猜想(a):
| 实验步骤 |
实验现象 |
实验结论 |