下表是空气中的气体成分和人体呼出的气体成分含量对照表:
| 气体成分 |
氮气 |
氧气 |
二氧化碳 |
水 |
其他气体 |
| 空气中的气体(﹪) |
78 |
21 |
0.03 |
0.07 |
0.9 |
| 呼出的气体(﹪) |
78 |
16 |
4 |
1.1 |
0.9 |
某校研究性学习小组的同学设计了简单的实验方案,验证呼出的气体与吸入的气体成分的含量有什么不同,其四个主要操作步骤如图(1、2、3、4)所示,请依据图示将主要实验操作步骤及验证依据填入下表中的空白处: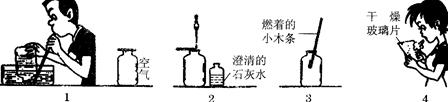
| 实验步骤 |
验证依据 |
| 1、用排水法收集两瓶呼出的气体,另收集两瓶空气。 |
|
| 2、将澄清石灰水分别滴入盛有呼出的气体和空气的集气瓶中。 |
根据,判断二氧化碳含量不同。 |
| 3、 。 |
根据木条燃烧情况的不同,判断氧气含量不同。 |
| 4、 。 |
根据,判断水含量不同。 |
酷爱化学的小明同学在家里建立了自己的小小化学实验室,下图是他平时收集的部分实验仪器和装置,请填空: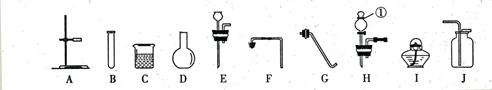
〔1〕仪器①的名称是: 。
〔2〕小明准备用双氧水制取氧气,为便于控制反应速率而获得平稳的氧气流,则他的发生装置和收集装置应选择图中的 (填字母),反应的化学方程式为 。
〔3〕小明还设计了一套制取少量蒸馏水的简易装置,他已经选择了B和C,则他还需选择 (填字母)。
〔4〕正上高三的姐姐告诉小明可利用图中的A、B、G、I来组装一套实验室制取甲烷的装置,小明据此推测实验室制取甲烷的反应原理应为下列方法中的 (填序号)①加热无水乙酸钠和碱石灰的固体混合物②常温下碳化铝和水反应③CO和H2在催化剂的作用下反应 ④将某些有机物在隔绝空气的条件下发酵
〔5〕小明和小亮还在家里做了如下实验,将过量的Na2CO3溶液滴入到一定量的CuSO4溶液中,有蓝色沉淀物生成。针对蓝色沉淀物的成分,他们展开了探究:
〖提出猜想〗经过讨论后,他们提出了三种猜想:
猜想一:沉淀物为CuCO3理由是(用化学方程式表示):
猜想二:沉淀物为Cu(OH)2 , 理由:根据Na2CO3溶液的酸碱性可判断Na2CO3溶液中一定存在着(填离子符号) 。
猜想三:沉淀物为:
〖查阅资料〗CuCO3和Cu(OH)2均为蓝色固体,不溶于水。受热后均会分解,各自生成对应的两种氧化物。
〖设计与实验〗小明设计了如下实验方案,并进行了实验:
第一步:将反应后的固液混合物经过滤、 并晾干后得蓝色固体;
第二步:将下列装置按照 A→B→C的顺序连接并进行实验,发现B中澄清石灰水变浑浊,C中白色粉末变蓝。于是小明认为猜想三是正确的。
〖反思与评价〗小亮认为小明得出的实验结论是不科学的,他的理由是: 。于是小亮提出了他的改进方法:将上图按照 的顺序连接并进行实验,若实验现象同上,则猜想三是正确的。
小华同学在观察课本实验“燃烧的条件”(图1)时,对产生的大量白烟产生了疑问。于是查阅资料:
【查阅资料】:……产物是白色固体——五氧化二磷。五氧化二磷会刺激人体呼吸道,在空气中可能与水蒸气反应,生成一种剧毒物质——HPO2(偏磷酸)由小华查阅的资料看,他最初的疑问可能是_________________________________;
分析:P2O5和偏磷酸都会伤害人的身体,应对此实验进行改进。
【实验改进】:小明与同学一起对课本实验进行了如下改进(图2),去掉铜片,将足量的红磷和白磷分别放在两个大试管中,在试管口各自套一个瘪气球,用线固定。然后将两支试管同时浸在盛有热水的烧杯中。
【观察现象】:可观察到试管中_______________________________。
【得出结论】:可燃物的燃烧必须具备的条件是温度达到着火点,跟空气(或氧气)接触
【反思与评价】:改进后的装置与原装置比较,其优点为_____________________。
【实验创新】:待发生反应的试管冷却后,小明将试管倒立在水中(试管口接近液面),握住气球口部,小心取下气球,观察试管中的现象是_____________________________;小明进行此实验的目的是_________________。
某课外小组的同学将玻璃罩内充满纯净的二氧化碳气体,如图A所示,在光照充足的条件下,经过一段时间后,该小组同学用注射器从a处抽取气体,测定玻璃罩内气体的成分及其含量。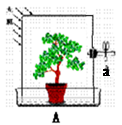
【查阅资料】①植物通过光合作用吸收二氧化碳气体,放出氧气。
②氢氧化钠和氢氧化钙性质相似,其水溶液都能与二氧化碳发生反应,
且没有气体物质生成。
【实验一】检验玻璃罩内是否含有二氧化碳气体?
| 实验步骤 |
实验现象 |
实验结论 |
| 抽取适量气体,注入石灰水中 |
玻璃罩内含有二氧化碳。 |
|
发生的化学方程式为 |
【实验二】采用两种方法测定玻璃罩内气体中氧气的含量。
方法1:用如图B所示的装置测量气体中氧气的含量。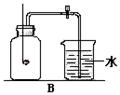
(1)实验前对该装置的气密性进行检查,小明设计了一种方法,请你帮他完成:打开止水夹,把导管末端浸没在水中,,若导管内水柱下降,则装置气密性良好;
(2)将抽取出的气体用排水法收集到150 ml的集气瓶中,关闭止水夹,点燃红磷;
(3)待装置冷却到室温后,打开止水夹,烧杯中的液体进入集气瓶中,体积约为100 ml。
方法2:用如下图C所示的装置测量气体中氧气的含量。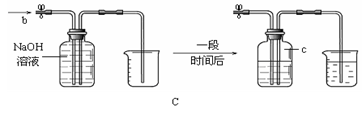
(1)抽取150 ml的气体,缓缓地从b处通入装置中;
(2)实验结束后,c处气体的化学式为,集气瓶中排出液体的体积约为75 ml,该方法所测得氧气约占气体总体积的%。
【实验反思】通过对比,该小组同学发现,两种方法所得实验结果差距较大,其中实验结果更准确的是(填写“方法1”或“方法2”)。36. 10升; 15.8%
据长沙新闻媒体报道,最近使用燃气热水器不当引起煤气中毒事故,造成不必要的人员伤亡,煤气是由燃气不充分燃烧后产生的,煤气的主要成分有
、水煤气和
.这些事故引起了我市中学生的广泛关注,某中学化学兴趣小组对燃气的燃烧进行科学探究.
(1)
使人中毒的原因是.
(2)你如何从事故现场收集一瓶煤气?.
证明煤气中一定含有
(没有足量的煤气供实验证明使用).
你所设计的实验方案为(只要求写简单的实验步骤):
①;
②;
③;
④;
⑤.
(以上空格可不填满)