有Al、CuO、Fe2O3组成的混合物共10.0 g,放入500 mL某浓度的盐酸溶液中,混合物完全溶解,当再加入250 mL 2.0 mol/L的NaOH溶液时,得到的沉淀最多。上述盐酸溶液的液度为
| A.0.5 mol/L | B.3.0 mol/L | C.2.0 mol/L | D.1.0 mol/L |
现有四种元素的基态原子的电子排布式如下:①ls22s22p63s23p4②ls22s22p63s23p3③ls22s22p3④ls22s22p5 , 则下列有关比较中正确的是
| A.第一电离能:④>③>②>① | B.原子半径:④>③>②>① |
| C.电负性:④>③>②>① | D.最高正化合价:④>③=②>① |
已知[ZnCl4]2-中Zn2+的4s轨道和4p轨道形成sp3型杂化轨道,则[ZnCl4]2-的空间构型为
| A.直线形 | B.平面三角形 |
| C.平面正方形 | D.正四面体形 |
据权威刊物报道,1996年科学家在宇宙中发现H3分子。甲、乙、丙、丁四位学生对此报道的认识正确的是
| A.甲认为上述发现绝对不可能,因为H3分子违背了共价键理论 |
| B.乙认为宇宙中还可能存在另一种氢单质,因为氢元素有三种同位素必然有三种同素异形体 |
| C.丙认为H3分子实质上是H2分子与H+以特殊共价键结合的产物,应写成H3+ |
| D.丁认为如果上述发现存在,则证明传统的价键理论有一定的局限性,有待继续发展 |
对于SO2和CO2说法正确的是
| A.都是直线形结构 |
| B.中心原子都采用sp杂化 |
| C.S原子和C原子上都没有孤对电子 |
| D.SO2为V形结构,CO2为直线形结构 |
根据键能数据估算CH4 (g)+4F2 (g)=CF4(g)+4HF(g)的反应热ΔH为
| 化学键 |
C—H |
C—F |
H—F |
F—F |
键能/(kJ·mol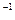 ) ) |
414 |
489 |
565 |
155 |
| A.–1940 kJ · mol-1 | B.+1940 kJ · mol-1 |
| C.–485 kJ · mol-1 | D.+485 kJ · mol-1 |