用下图Ⅰ所示装置通电10分钟后,去掉直流电源,连接成图Ⅱ所示装置,可观察到U形管左端铁电极表面析出白色胶状物质,U形管右端液面上升。下列说法正确的是 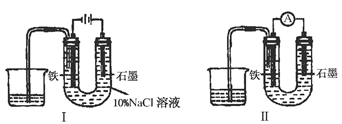
| A.同温、同压下,装置Ⅰ中石墨电极上方得到的气体比铁电极上方得到的气体多 |
| B.用装置Ⅱ进行实验时铁电极的电极反应为Fe-2e-+2OH-===Fe(OH)2 |
| C.用装置Ⅱ进行实验时石墨电极的电极反应为2H++2e-===H2↑ |
| D.装置Ⅰ通电10分钟后铁电极周围溶液pH降低 |
互为同分异构体的物质不可能 ()
| A.具有相同的相对分子质量 | B.具有相同的结构 |
| C.具有相同的通式 | D.具有相同的分子式 |
正丁烷与异丁烷互为同分异构体的依据是()
| A.具有相似的化学性质 |
| B.具有相同的物理性质 |
| C.分子具有相同的空间结构 |
| D.分子式相同,但分子内碳原子的结构方式不同 |
下列性质中,可以证明某化合物内一定存在离子键的是
| A.可溶于水 | B.具有较高的熔点 |
| C.水溶液能导电 | D.熔融状态能导电 |
下列哪组元素的原子之间反应容易形成离子键
| 原子 |
a |
b |
c |
d |
e |
f |
g |
| M电子层 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
A、a和c B、a和f C、b和g D、d和g
M元素的1个原子失去2个电子,该2个电子转移到Y元素的2个原子中去,形成离子化合物乙,下列说法中,正确的是
| A.熔融的Z能导电 | B.乙可以表示为M2Y |
| C.乙一定溶于水 | D.M形成+2价阳离子 |