某课外小组的同学收集了含水蒸气、一氧化碳和二氧化碳的废气,为确认这种废气中存在CO,他们在实验室按下图所示装置进行实验〔气体通过装置A速度很慢,假设在此处发生的反应完全;碱石灰(CaO和NaOH的混合物)过量〕。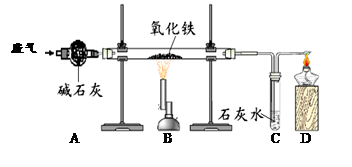
(1)A中碱石灰的作用是___________________________。
(2)B中发生反应的化学方程式是______________________________________。
(3)该实验能证明混合气体中存在CO的现象是 。
(4)若反应前称得硬质玻璃管内的氧化铁质量为10克,反应一段时间后冷却再次称量发现硬质玻璃管内的固体质量变为7.6克,则反应了的氧化铁的质量分数为____________。
维生素C又名抗坏血酸,易溶于水,易被氧化,能与碘反应.人体缺乏维生素C可引发多种疾病.某研究性学习小组对它研究如下:
(1)猜想:维生素C可能具有酸性.
(2)实验方案:提供的试剂有维生素C片、蒸馏水、紫色石蕊溶液、无色酚酞溶液、氢氧化钠溶液、pH试纸.(实验仪器自选)
根据以上用品,请你帮助他们设计出两种实验方案,并写出实验现象:
| 实验内容 |
实验内容 |
实验现象 |
| 方案I |
||
| 方案Ⅱ |
(3)结论:维生素C具有酸性.根据维生素C的性质,判断下列物质中能与维生素C反应的是()
(A)金属镁
(B)氯化钾
(C)氢氧化钠
(D)硫酸铜
(4)某同学联想到西红柿等蔬菜、水果中含有丰富的维生素C,则其放置时间的长短是否对维生素C的含量产生影响?他设计了如下的实验方案:
Ⅰ.把新鲜西红柿和放置一周的西红柿分别捣碎,用纱布将汁液挤入两个烧杯中.
Ⅱ.取两支盛有2mL蓝色的碘的淀粉溶液的试管,分别滴加上述两种汁液,边加边振荡,直到蓝色刚好消失,记录滴数如下:
| 汁液 |
新鲜西红柿的汁液 |
放置一周的西红柿的汁液 |
| 滴数 |
12 |
20 |
请回答下列问题:
①你认为维生素C含量较高的是________.
②你从中得到的启示是________________________.
葡萄糖是生命体所需能量的主要来源.
[提出问题]葡萄糖的完全燃烧产物是CO2和H2O,由此能否证明葡萄糖是只由碳元素和氢元素组成的有机物?
[实验设计]为了确定葡萄糖的元素组成,某小组设计了如下实验(其中浓硫酸、无水CaCl2均为常用干燥剂,部分固定装置省略).
(1)装置A中发生反应的化学方程式是________________________.
(2)装置B中浓硫酸的作用是________________________.
(3)装置C处氧化铜的作用是________________________.
[方案评价]
(1)用充有空气的储气球代替装置A,是否更有利于实验的进行?________(填“是”或“否”),原因是________________________________.
(2)装置C处葡萄糖燃烧的设计特点是________________________________________(至少写1条).
[数据处理]下表是同学们填写的实验报告,请你帮助完成.
| 实验事实 |
数据分析及结论 |
| 1.8g葡萄糖完全燃烧,得到2.64g CO2和1.08g H2O |
数据分析:________________ ________________________ ________________________ 结论:葡萄糖含有C、H、O三种元素 |
[讨论交流]为了尽量减少误差:
(1)该实验在进行过程中应注意的问题是________________________________________
____________________________________________________________________(写1条).
(2)从定量实验的角度看,该实验可进一步改进,请简要写出一个改进意见:________
________________________________________________________________________.
某同学家中有一袋化肥,可能混入了其他化肥,且化肥包装袋上的字迹模糊.该同学进行了如下探究,请你参与探究并填空:
[提出问题]该化肥中含有什么物质?
[收集信息]经询问得知,该化肥为铵态氮肥.
[提出猜想]该化肥所含的阴离子可能是Cl-、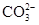 、
、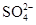 ;中的一种或几种.
;中的一种或几种.
[实验、记录与分析]
| 实验操作步骤 |
实验现象 |
实验分析 |
| (1)取少量该化肥样品和少量熟石灰放在研钵中混合研磨 |
________ |
含有铵根离子 |
| (2)另取少量该化肥样品于试管中,加入适量的水完全溶解,滴加足量的硝酸钡溶液,再滴加少量稀硝酸,过滤 |
产生白色沉淀,沉淀不溶解 |
没有________(填化学式)存在 |
| (3)取(2)中所得滤液少量于试管中,滴加________ |
________ |
有Cl-存在 |
[实验结论]若该化肥中只含有一种阳离子,则其中一定含有的物质是(写化学式)________________________________________________________________________.
[实验反思]若步骤(2)中用氯化钡溶液代替硝酸钡溶液是否可行?________(填“是”或“否”),请简要说明原因:________________________________________.
实验室有一瓶化肥的标签已脱落,只知道它是NH4Cl、(NH4)2SO4、NH4HCO3和尿素[CO(NH2)2]中的一种.请你完成以下探究:
[猜想]猜想①:该化肥是NH4Cl,
猜想②:该化肥是________,
猜想③:该化肥是NH4HCO3,
猜想④:该化肥是尿素.
[实验探究]
(1)取少量样品在研钵中与熟石灰研磨,有刺激性气味的气体放出,证明猜想________不成立;写出其中一种化肥发生该反应的化学方程式:
________________________________________________________________________.
(2)如图1,另取少量样品于试管中,滴加适量水振荡,再选图2中________滴入试管中,若无气泡放出,则猜想________不成立.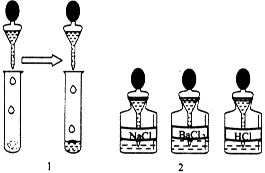
(3)在步骤(2)的试管中再滴入图2中的________,若________,则猜想①成立;若________,则猜想②成立,其反应的化学方程式为________________________________________
________________________________________________________________________.
无土栽培是利用营养液栽培作物的一种方法.
(1)下列化学肥料中属于复合肥的是________(填序号).
①硝酸铵
②磷酸二氢铵
③硝酸钾
④硫酸钾
(2)某同学要在实验室配制150g溶质质量分数为2%的硝酸钾溶液,需要硝酸钾的质量为________g.
(3)现有一种无色的营养液,可能由KNO3、Ca(NO3)2、K2CO3、KCl中的一种或几种物质组成,为探究其成分,某同学设计并完成了如下图所示的实验.
根据以上实验,请你进行有关推断.
①由实验1可确定原营养液中一定没有的物质是________________;
②根据实验1、实验2推测原营养液的组成可能有________种情况;
③若测得原营养液中K+和Cl-的数目之比为1︰1,则原营养液的组成中的溶质是________
________________________________________________________________________.