根据以下叙述回答。
能源可划分为一级能源和二级能源。自然界中以现成形式提供的能源称为一级能源;需依靠其他能源的能量间接制取的能源称为二级能源。氢气是一种高效而没有污染的二级能源,它可以由自然界中大量存在的水来制取:
(1)下列叙述正确的是( )
A.电能是二级能源 B.水力是二级能源
C.天然气是一级能源 D.水煤气是一级能源
(2)关于用水制取二级能源氢气,以下研究方向不正确的是( )
A.构成水的氢和氧都是可以燃烧的物质,因此可研究在水不分解的情况下,使氢成为二级能源
B.设法将太阳光聚焦,产生高温,使水分解产生氢气
C.寻找高效催化剂,使水分解产生氢气,同时释放能量
D.寻找特殊化学物质,用于开发廉价能源,以分解水制氢气
(3)1g氢气燃烧时约放热142.9kJ,而1kg汽油燃烧时约放热46000kJ。氢气被公认是21世纪替代矿物燃料的理想能源。你认为氢气作为能源的三个主要优点:_______________,________________,________________。
现有甲、乙两个容积相等的恒容密闭容器,向甲中通入6 mol A和2 mol B,向乙中通入1.5 mol A、0.5 mol B和3 mol C,将两容器的温度恒定为770 K,使反应3A (g) +B (g)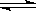 xC(g)达到平衡,此时测得甲、乙两容器中C的体积分数都为0.2。
xC(g)达到平衡,此时测得甲、乙两容器中C的体积分数都为0.2。
请回答下列问题:
(1)若平衡时,甲、乙两容器中A的物质的量相等,则x= ____________;若平衡时,甲、乙两容器中A的物质的量不相等,则x= ____________。
(2)平衡时,甲、乙两容器中A、B的物质的量之比是否相等?__________(填“相等”或“不相等”),平衡时甲中A的体积分数为________________。
(3)若平衡时两容器中的压强不相等,则两容器中压强之比为____________________。
一定温度下,将3molA气体和1molB气体通过一密闭容器中,发生如下反应:3A(g)+B (g) xC(g)。请填写下列空白:
xC(g)。请填写下列空白:
(1)若容器体积固定为2L,反应1min时测得剩余1.8molA,C的浓度为0.4mol/L。
①1min内,B的平均反应速率为_________;x=_________;
②若反应经2min达到平衡,平衡时C的浓度________0.8mol/L(填“大于”、“等于”或“小于”);
③平衡混合物中,C的体积分数为22%,则A的转化率是_________;
(2)若维持容器压强不变
①达到平衡时C的体积分数_________22%,(填“大于”、“等于”或“小于”);
②改变起始物质加入的量,欲使反应达到平衡时C的物质的量是原平衡的2倍,则应加入_________molA气体和_________molB气体。
 某温度(t℃)时,测得0.01mol·L-1的NaOH溶液的pH=11,则该温度下水的Kw=。在此温度下,将pH=a的NaOH溶液VaL与pH=b的H2SO4溶液VbL混合。
某温度(t℃)时,测得0.01mol·L-1的NaOH溶液的pH=11,则该温度下水的Kw=。在此温度下,将pH=a的NaOH溶液VaL与pH=b的H2SO4溶液VbL混合。
(1)若所得混合液为中性,且a=12,b=2,则Va︰Vb= 。
。
(2)若所得混合液为中性,且a+b=12,则Va︰Vb=。
(3)若所得混合液的pH=10,且a=12,b=2,则Va︰Vb=。
用如图所示的装置进行电解。A中盛有AgNO3溶液,B中盛有饱和Na2SO4溶液通电一会儿,发现湿润的淀粉KI试纸的C端变为蓝色。则:
(1)电源的F端为_____________极。
(2)A中发生反应的化学方程式为________________。
(3)在B中观察到的现象是____,_________,_________
(4)室温下,若从电解开始到时间t s,A、B装置中共收集到标准状况下的气体0.168L,,B中析出硫酸钠晶体(Na2SO4﹒10H2O) ωg。若电解过程中无其他副反应发生,经测定电解后,A中溶液体积恰为1000mL,则①A溶液的pH为______________。
②电解前饱和Na2SO4溶液的质量分数为________________(列出算式即可。)
已知:① C(s)+O2(g)=CO2(g);DH=—393.5 kJ·mol-1
② 2CO(g)+O2(g)=2CO2(g);DH=-566 kJ·mol-1
③ TiO2(s)+2Cl2(g)=TiCl4(s)+O2(g);DH=+141 kJ·mol-1
则TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的DH= 。
。