同学们通过查阅资料知道,过氧化氢分解反应的催化剂除二氧化锰外,还有氯化铁溶液、氯化铜溶液中的金属离子和土豆中含有的过氧化氢酶。同学们通过如下实验进行相关研究。
实验一:验证二氧化锰能加快过氧化氢的分解速率 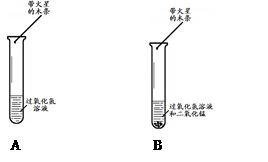
分别取5 mL 5%的过氧化氢溶液于两支试管中,向B中试管内加入少量二氧化锰(如上图所示)。A中带火星的木条不复燃,B中带火星的木条复燃,实验证明二氧化锰加快了过氧化氢的分解速率。A中木条不复燃的原因是 ,B中反应的化学方程式是 。
实验二:研究催化剂的某些因素对过氧化氢分解速率的影响
方案Ⅰ:分别取20 mL 5%的过氧化氢溶液于3个大小相同的锥形瓶中。向其中两个锥形瓶中分别加入含相同数目金属离子的氯化铁溶液和氯化铜溶液,分别连接传感器测体系压强(如右图所示)。测定数据如下表所示:
 时间/s 时间/s试剂 压强/KPa |
0 |
60 |
120 |
180 |
240 |
300 |
| 20mL 5%的过氧化氢溶液 |
101.86 |
102.99 |
103.42 |
103.67 |
103.99 |
104.00 |
| 加入氯化铁溶液 |
102.21 |
105.35 |
115.40 |
129.69 |
145.52 |
163.99 |
| 加入氯化铜溶液 |
101.50 |
102.73 |
107.53 |
114.78 |
122.49 |
130.39 |
(1)加入含相同数目金属离子的氯化铁溶液和氯化铜溶液,该步操作的实验目的是 。
(2)根据上表数据得出的结论是 。
方案Ⅱ:从同一部位取2个质量均为1.7 g的正方体土豆块,将其中一块切成若干片,片与片相连不断开,同时分别放入盛30 mL 5%过氧化氢溶液的50 mL量筒中。均看到有气泡生成,一段时间,只有土豆片不断上升。通过实验得出的结论是 。
【实验反思】通过实验一和实验二说明,测量不同的物理量可判断过氧化氢的分解速率。
下列做法中能比较过氧化氢的分解速率的是 (填选项序号)。
A. 测量完全反应后气体的总体积 B. 测量相同时间内产生气体的体积
C. 测量相同时间内体系压强的变化 D. 测量相同时间内溶液质量的变化
学习了MnO2对过氧化氢有催化作用的知识后。某同学想:CuO能否起到类似MnO2的催化剂作用呢?于是进行了如下探究。
【猜想】Ⅰ. CuO不是催化剂、也不参与反应,反应前后质量和化学性质不变;
Ⅱ. CuO参与反应产生O2,反应前后质量和化学性质发生了改变;
Ⅲ. CuO是反应的催化剂,反应前后_________ _____________________。
【实验】用天平称量0.2gCuO,取5ml5%的过氧化氢溶液于试管中,进行如下实验:

(1)填写下表:
| 步骤③现象 |
步骤⑥结果 |
步骤⑦现象 |
结论 |
| ___ _____带火星的木条复燃 |
____ _____ |
溶液中有气泡放出 _____ _______ |
猜想Ⅰ、Ⅱ不成立 猜想Ⅲ成立 |
(2)步骤①的目的________ ____________。
(3)步骤④需用到的实验仪器有:铁甲台(带铁圈)、漏斗、烧杯、_____ ____。
(4)过氧化氢能被CuO催化分解放出O2的化学方程式为___________________。
【拓展】要探究步骤⑤做过催化剂的CuO其它化学性质,还应补做的实验是______________
_____ __________________(写一种)。
某兴趣小组根据实验室提供的仪器和药品进行了氧气的制备实验。
(1)甲同学选用如右图所示的装置制取氧气。
①写出仪器B的名称:______。
②甲同学应选取的试剂是Mn02和_______(填化学式),
Mn02固体在该反应中起_______作用。
③除用排水法外,甲同学还可选择_____法收集氧气。
④实验前,甲同学先向仪器A中加入水,然后将导管放人水槽中,并打开仪器A的活塞,观察导管口是否有连续的气泡出现。该实验操作的目的是__________。
(2)乙同学称取一定质量KMn04放在大试管中,将温度控制在250℃加热制取O2,该反
应的化学方程式为________。实验结束时,乙同学发现收集到的O2大于理论产量,针对这一现象,同学们进行了如下探究:
【提出猜想】猜想l:反应生成的MnO2分解放出02;
猜想Ⅱ:反应生成的K2Mn04分解放出O2
做出上述猜想的理由是_______。
【实验验证】同学们分为两组,分别进行以下实验:
①第一组同学取一定质量的Mn02,在250℃条件下加热一段时间,冷却后
测得Mn02的质量不变。则猜想________________错误。
②第二组同学取K2Mn04在250℃条件下加热,没有用测定质量的方法得
出了猜想Ⅱ正确的结论。该组同学选择的实验方法是_________________ 。
【拓展延伸】实验发现,K2MnO4受热只能部分分解,经分析可能是生成物K2O对其分
解产生影响。请设计实验方案验证:________________。
【实验反思】通过以上实验探究,你对“问题的发现与解决”有何认识?_________。
食品着色剂、食品香料等食品添加剂,在规定范围内使用是安全的,可明显提高食品的感官质量,满足人们不同的需要;而苏丹红、三聚氰胺、瘦肉精根本不是食品添加剂,是违法添加物。食品安全,人人有责。丹丹同学发现妈妈做早餐包子、馒头时,向面团中加入发酵粉,蒸出的包子、馒头中有许多小孔,松软可口,丹丹同学对发酵粉产生了兴趣。
⑴提出问题:发酵粉的主要成分是什么物质?
⑵查阅资料:含钠元素的物质在酒精灯的火焰上灼烧时,会产生黄色火焰。
⑶实验探究:下面是丹丹同学设计的探究实验,请你帮她完成。
①将发酵粉取样,在酒精灯的火焰上灼烧产生黄色火焰。
②取样于试管中,加入稀盐酸,产生大量的气泡,将该气体通入澄清石灰水,澄清的石灰水变浑浊,则发酵粉的主要成分中含有的离子是 (写离子符号)。
⑷小结与思考:
①发酵粉的主要成分是 (写化学式)。
②发酵粉与面粉、水混合发酵产生CO2气体,这些气体会在面团中形成许多小孔,使包子、馒头松软可口。
③实验室制取CO2可选择下列装置中的(填字母序号,任写一组)。

④实验室用A装置制取氧气的化学方程式为。E装置内装满水收集氧气时,还可用于测定氧气的体积,此时还需要(填仪器名称),氧气由(填“a”或“b”)进入E中。
2011年是国际化学年(IYC2011),其宗旨是"增进公众对化学重要性的认识,鼓励青年人热爱化学,学习和研究化学"。某校化学兴趣小组的同学,对课本中一氧化碳还原氧化铁实验作了绿色化改进后制取单质铁(
,
是活塞):
(1)关闭
、开启
,可以验证
还原
的产物。
①这是关于气体的实验,实验前必须对装置进行
② 还原 的化学方程式为
③在e处点燃气体的目的是
(2)关闭
,开启
,可以将
口出来的气体再从a通人装置而循环使用。
①
瓶中应装(填序号)。
| A. | 澄清石灰水 | B. | 水 | C. | 石蕊溶液 | D. | 浓硫酸 |
②反应完后(假设b瓶中
全部转化为纯碱),要从
瓶中溶液得到纯碱固体,必要的实验操作为转移、结晶。
③该实验这样改进的主要优点是
(11分) 在高效复习课堂中,同学们利用“硫酸、硝酸钡、氢氧化钠、碳酸钾” 四种物质的溶液对 “复分解反应发生的条件”进行再探究。
【知识回放】
通过判断上述四种溶液两两之间能否发生反应,我能写出其中符合下列条件的两个化学方程式:
⑴一个中和反应 ① ;
⑵一个有沉淀生成的反应 ② 。
【挖掘实质】
(1)图1是HCl和NaOH在水中解离出离子的示意图,我发现HCl在水中会解离出H+和Cl-,NaOH在水中会解离出Na+和OH-,以此类推硝酸钡在水中会解离出的离子是③(填离子符号)。
(2)图2是稀盐酸和氢氧化钠溶液发生化学反应的微观过程示意图,该化学反应的实质可以表示为H++ OH-=H2O,我也能用同样的方式表示上述四种溶液两两之间发生反应时有气体生成的反应的实质④。
(3)通过探究上述四种溶液两两之间是否发生反应的实质,我发现NaOH和H2SO4溶液能发生复分解反应,因为溶液中的H+和OH—不能大量共存;⑤溶液和⑥溶液也可以发生复分解反应(任写一组物质,下同),因为⑦;⑧和⑨溶液不能发生复分解反应,因为⑩(填离子符号,下同)也不能大量共存。
【知识升华】
通过对“复分解反应发生的条件”的再探究,我得出复分解反应发生条件的实质是11。