(7 分)小明上网阅读时得知根据氨气还原氧化铜的反应,可设计测定铜元素相对原子质量(Ar)的实验。小明很感兴趣,和化学兴趣小组的同学设计了如下探究活动,请结合下图回答问题。
(1)实验室利用氯化铵和氢氧化钙固体之间的复分解反应制取氨气。小明将A与E连接,观察到无色酚酞试液变红,说明氨气显 (填“酸性”、“中性”、或“碱性”)。A中发生反应的化学方程式为 。
(2)小刚将纯净干燥的氨气通入B中,观察到玻璃管内黑色固体变为亮红色,管口有液滴,同时生成空气中含量最多的气体,B中发生反应的化学方程式为 。
(3)小组同学测定铜元素相对原子质量(Ar)的实验设想是:先称量反应物CuO的质量M(CuO),反应完全后测定生成物水的质量M(H2O),由此计算出Cu的相对原子质量。
①小组每位同学从所提供的仪器中选择并组装了一套用于本实验的装置,其中简单、合理的是(填序号,装置可重复使用) 。
A.acdbbeecd B.aeebbcdee C.aeebbeecd D.abbeecd
②在本实验中,使测定结果Ar(Cu)偏大的是_______________ (填序号);
A.CuO未完全起反应
B.CuO不干燥
C.氢氧化钠固体不干燥
D.CuO中混有不反应的杂质
E.NH4C1与Ca(OH)2混合物不干燥
③在本实验中,还通过测定_______________和_____________的质量达到目的。
某化学兴趣小组进行溶液的配制和粗盐的初步提纯实验。
(1)配制200g质量分数为8%的氢氧化钠溶液:
①计算:需要氢氧化钠固体的质量为克,需要水的体积为mL(水的密度近似看作1g/mL)。
②称量:调节托盘天平平衡,将一个烧杯放在托盘天平的盘,称量其质量。然后(按操作的先后顺序选填字母),直至天平平衡。
A.将氢氧化钠固体加入烧杯中 B.按需要添加砝码、移动游码
该步骤中用烧杯而不用纸称量氢氧化钠的原因是。
③用量取所需要的水,倒入盛有氢氧化钠固体的烧杯中,用搅拌,使其溶解,并冷却到室温。
④将配制好的溶液放入试剂瓶,塞好橡胶塞并,放到指定的地方。
(2)粗盐的初步提纯:
①称取5.0克粗盐,用药匙逐渐加入到10mL水中,直到粗盐不再溶解为止。还需进行的实验操作步骤的顺序为:称量剩余粗盐、(填编号)。
A.过滤 B.计算产率 C.蒸发 D.称量精盐
②过滤操作如右图所示,指出其中的错误之处:
;;
;。
(16分)请你参与下列探究。
【问题情景】某化学实验小组同学将铁粉投入硫酸铜溶液中,发现生成红色固体物质的同时,有较多的气泡放出。这一现象激发起同学们的探究欲望,生成的是什么气体呢?
【提出猜想】从物质组成元素的角度分析,放出的气体可能是SO2、O2、H2。
【查阅资料】SO2易溶于水,它能与NaOH溶液反应,生成Na2SO3。
【方案设计】依据上述猜想,实验小组同学分别设计了如下方案:
(1)甲同学认为是O2,则检验方法是。
(2)乙同学认为是SO2,则只需将放出的气体通入盛有NaOH溶液的洗气瓶中,称量通气前后洗气瓶的质量。写出SO2与NaOH反应的化学方程式:。
(3)实验小组同学合作设计了如下组合实验方案,排除和验证猜想的气体。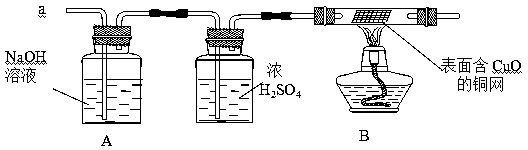
如果放出的是O2和H2的混合物,你认为方案中的安全隐患是。
丙同学认为:为确保安全,实验前应先进行验纯操作。
【实验探究】经丙同学确认安全后,小组同学首先对装置A进行称量,再将收集到的气体从a通入,过一会儿点燃B处酒精灯;一段时间后,发现表面含CuO的铜网由黑色变为光亮的红色;停止通气,再次称量装置A,发现质量不变。
结论:(1)铁粉与硫酸铜溶液反应时,产生的气体是 。
(2)写出该气体与CuO反应的化学方程式:。
【思维拓展】
(1) 由上述实验可以推出,硫酸铜溶液显 (选填“酸”或“碱”)性。
(2) 不通过称量,如何判断SO2与NaOH溶液发生了反应呢?有一同学设计了右图所示的装置进行实验,发现试管内液面上升,就得出SO2与NaOH溶液发生反应的结论。其他同学认为这一方案不严谨,理由是 。要得到科学严谨的结论,仍利用该装置,补做的实验是。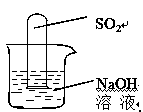
(10分)某兴趣小组利用下列装置进行实验,请回答: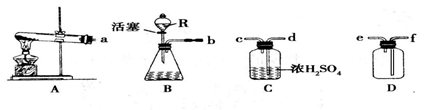
(1)R仪器的名称是,用过氧化氢制氧气应选用的发生装置是(填序号,下同),分解过氧化氢制得的氧气常带有少量水蒸气,欲收集一瓶干燥的氧气,经过的导气管口正确的连接顺序是b接()()()()
(2)若B装置中装有石灰石和稀盐酸,则该装置可用于制取气体。收集该气体时通常用法收集。制这种气体的化学方程式是。
乙醇是以高粱、玉米、薯类等为原料,经发酵、蒸馏制得,属于可再生能源。在汽油中加入适量乙醇作为汽油燃料,可节省石油资源,减少汽车尾气的污染。2001年4月2日国家技术监督局发布《车用乙醇汽油国家标准》并于同年4月15日开始实施。
乙醇( )完全燃烧时生成
)完全燃烧时生成 。如果氧气不足,乙醇燃烧可生成多种物质。现用下图装置进行实验,确证乙醇燃烧产物中有CO、
。如果氧气不足,乙醇燃烧可生成多种物质。现用下图装置进行实验,确证乙醇燃烧产物中有CO、 和
和 。
。
请回答下列问题:
(1)能确证产物中有 的现象是________________________;能确证产物中有CO的现象是_______________________________。
的现象是________________________;能确证产物中有CO的现象是_______________________________。
(2)实验时,可观察到装置B中石灰水变浑浊,D中石灰水无变化。B装置的作用是___________________________________;C装置的作用是_______________________;D装置的作用是___________________________________________。
(3)为了保护环境,应在装置的排气管口采取的措施是________________________。
根据下列实验装置图,请回答下列相关问题:
(1)写出仪器①、②的名称①____________,②____________;
(2)装置A中所发生反应的化学方程式为______________________;
(3)装置B的作用是吸收装置A中挥发出来的HCl;装置C中浓硫酸的作用是________________________________________;
(4)反应一段时间后,装置F的玻璃管中可观察到的现象是_____________________;装置中澄清石灰水变浑浊,请写出该反应的化学方程式________________________;
(5)某学生在验证CuO与CO的反应产物时,在装置E中加入一种试剂。你认为该试剂是________________________________________。