暑假,同学们在帮忙老师整理实验室时,发现一瓶石灰水试剂瓶瓶壁和瓶塞周围有一些白色粉末。为了弄清楚白色粉末的成分及形成原因,他们进行了如下探究:
(1)对白色粉末成分的猜想和成因分析:
| 白色粉末的成分 |
形成的原因 |
| 可能是CaCO3 |
石灰水与空气中CO2反应; 化学方程式为: |
| 可能是 |
暑假气温较高,溶质的溶解度降低或溶剂蒸发,石灰水中的溶质结晶析出 |
经过反复思考,同学们认为白色粉末还可能是 的混合物。
(2)设计实验:
甲同学取白色粉末装入试管中,加入少量的水、振荡,发现有白色固体不溶解。于是他得出粉末中一定有CaCO3的结论。乙同学查阅了溶解性表(如下表),认为甲同学的结论不严密,理由是: 。
| |
OH- |
Cl- |
CO32- |
NO3- |
| Ca2+ |
微 |
溶 |
不 |
溶 |
为了得出较严密的结论,他们进行了如下实验,请完成下列实验报告:
| 实验步骤 |
可能观察到的现象 |
结论 |
| ①取上述试管中上层清液,滴加1~2滴无色酚酞试液 |
① 。 |
② 。 |
| ②往上述试管中的残留的固体中加入稀盐酸 |
③ 。 |
④白色粉末中 (选填“有”或“无”)CaCO3 |
| ③由上述实验可知白色粉末的成分是: 。 |
(3)交流与反思:
通过上述实验的探究,同学们向实验室提出保存、使用易变质的溶液时的下列建议,合理的是 (选填序号)。
A.密封保存 B.使用前,临时配制 C.禁止使用这种试剂
(7分)某班同学做验证铁、铜、银的金属活动性顺序的实验,用到的药品有铁丝、铜丝、银丝、稀硫酸和硫酸铜溶液。实验结束后,化学兴趣小组的同学欲对该实验的废液进行探究,请你一起参与。
【提出问题】废液中含有什么物质?
【交流表达】(1)小明通过观察,认为废液中一定含有硫酸铜。他观察到的现象是_____。
(2)小红通过分析,认为废液中一定含有硫酸亚铁,她的依据是______________________。
【作出猜想】小华认为废液中还可能含有硫酸。
【实验验证】(1)小华测得废液的pH小于7,证明废液中含有硫酸。用pH试纸测定溶液pH的方法是________________________________________________________________。
(2)小明取少量废液,向其中滴加氢氧化钠溶液,也得到了相同的结论。小明的实验现象是_______________________________。通过分析与实验,同学们得出废液中含有硫酸亚铁、硫酸铜和硫酸。
【拓展应用】
(1)若将废液中的溶质全部转化为硫酸亚铁,应向废液中加入过量的______________。写出该反应过程中的一个化学方程式______________________________________________。
(2)反应完全后,过滤,滤渣中物质为________________,滤液中溶质为硫酸亚铁。
如图所示为实验室常用的实验装置:
据图回答下列问题:
(1)写出带有标号的仪器名称:①,②。
(2)实验室通常用石灰石与稀盐酸反应制取二氧化碳,应选用的发生装置是(填序号,
下同),收集装置是。该反应的文字表达式为。
(3)F装置可用来测量生成的二氧化碳气体的体积,其中在水面上防一层植物油的目的
是,植物油上方原有的空气对实验的结果(填“有”或“没有”)明
显影响。
(4)实验室用高锰酸钾(KMnO4)制取氧气,应选用的发生装置是,收集装置是。该反应的文字表达式为。该反应属于 _______ 基本反应类型。
(5)某同学称取一定质量KMnO4放在大试管中,将温度控制在250℃加热制取O2,实验结束时,该同学发现收集到的O2大于理论产量,针对这一现象,同学们进行了如下探究:
【提出猜想】猜想l:反应生成的MnO2分解放出O2;猜想Ⅱ:反应生成的锰酸钾(K2MnO4)
分解放出O2做出上述猜想的理由是____________________________ 。
【实验验证】同学们分为两组,分别进行以下实验:
①第一组同学取一定质量的MnO2,在250℃条件下加热一段时间,冷却后测得MnO2的质量不变。则猜想_______错误。
②第二组同学取K2MnO4在250℃条件下加热,没有用测定质量的方法,也得出了猜想Ⅱ正确的结论。该组同学选择的实验方法是______________________________________ 。
【拓展延伸】实验发现,K2MnO4受热只能部分分解,经分析可能是生成物氧化钾(K2O)
对其分解产生影响。请设计实验方案验证:______________________________。
【实验反思】通过以上实验探究,该生对“问题的发现与解决”有何认识:必须通过认真分析,
用实验来加以证明。
某学校科学兴趣小组想设计一个实验,来模拟研究
:浓度增加是否增大地球"温室效应".他们查阅了有关数据: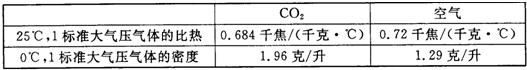
并设计了下面的实验和操作步骤:
Ⅰ、在两只同样的玻璃瓶里分别充满
和空气,并编号为甲、乙,塞紧带有同样温度计的橡皮塞.再把两只玻璃瓶放在阳光下照射(如右图),观察甲、乙瓶中的温度变化.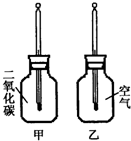
Ⅱ、阳光持续照射,间隔一定时间测量两玻璃瓶温度值,并记录
(见下表)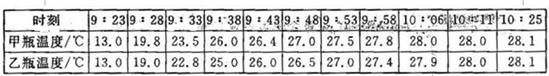
请回答下列问题:
(1)写出实验室制取
的化学方程式.
(2)往瓶中充
时,验证瓶中已充满了
的方法是
(3)该实验中,照射同样时间,根据上表的数据,比较甲、乙瓶温度变化的规律是
(4)该实验中,在阳光照射下,影响甲、乙瓶温度不同的原因,除了 的温室效应以外,还有的可能原因是(写出一点即可)
(5)有同学认为根据该模拟实验的目的,实验设计存在问题,你认为是(写出一点即可) .

⑴若试管中的药品是碳酸氢铵,观察到色固体逐渐,试管口有,且有气味的气体产生,如将产生气体通入澄清石灰水将会看到。
⑵由此实验可知,碳酸氢铵贮存时应注意
⑶若试管中的药品为铜绿,则观察到色固体逐渐变,是因为生成了(填物质名称)
⑷加热过程中试管破裂,可能的原因是(写两点)
某兴趣小组对上述固体酒精充分燃烧后残留的白色固体的成分进行丁如下探究。
【查阅资料】
(1)醋酸钙[
],不可燃.不助燃.易溶于水,溶于水时温度无显著变化;
(2)醋酸钙受热分解生成碳酸钙和有特殊气昧的丙酮;
【猜想与假设】
假设l:白色固体中含有
:假设2:白色固体中含有
假设3:白色固体中含有
假设4:白色固体中含有
【实验探究】
实验①:取少量白色固体溶于足量蒸馏水中,过滤,得到溶液和白色不溶物,
实验②:取①中滤液于试管中,滴入2滴酚酞试液.溶液变为红色;
实验③:取①中滤液于试管中,滴加碳酸钠溶液,有白色沉淀生成。
【交流讨论】
(1)根据实验①,甲同学认为假设2成立.理由是:;
(2)根据实验②,乙同学认为假设4成立。丙同学认为假设4不一定成立,但假设3成立.
因为丙同学在实验①中还发现:。
(3)仅根据实验③,丁同学认为假设3或假设4成立.但戍同学反对.理由是:;
(4)欲确认假设I成立,还需进行如下实验:
【反思提高】
写出实验③中有关反应的化学方程式:。