某含碳、氢、氧的有机物A能发生如下变化: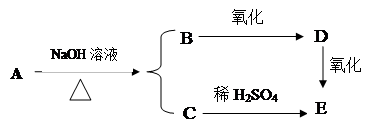
已知A、C、D、E均能发生银镜反应。试写出A、B、C、D、E的结构简式:
A B C D E
据中国地震台网测定,3月30日在贵州省黔东南苗族侗族自治州发生5.5级地震,据了解,这已经是贵州这个月以来发生的第三次地震。饮用水安全在灾后重建中占有极为重要的地位,为防止灾后疫病使用了大量的各种消毒液,如NaClO溶液,为防止灾后疫病使用了大量的各种消毒液,如NaClO溶液,某学习小组对消毒液次氯酸钠(NaClO)的制备与性质进行研究。
(1)下面是某同学从超市购买的某品牌消毒液包装说明查询到的部分内容:主要有效成分为次氯酸钠,有效氯含量8 000~ 10 000 mg/L。可用于各类家居用品、餐具、棉织衣物等的消毒,对彩色织物可能有褪色作用。本品须密封,置阴凉暗处保存。据此分析:
①室温时,他测得该消毒液(NaClO)的pH_______7(填“>”、“=”或“<”),其原因为(用离子方程式表示)_________________________。
②该消毒液还具有的化学性质有____(填序号)
| A.强氧化性 | B.强还原性 | C.不稳定性 | D.漂白性 |
③从该消毒液的保存要求分析,导致其失效的主要原因是(用化学方程式表示)____________________。
④日常生活中也常用明矾作净水剂,用离子方程式表示其净水原理___________________。
(2)该学习小组同学用石墨和饱和食盐水设计了如图所示的装置,进行消毒液( NaClO 溶液)制备,通电时,电解饱和食盐水的化学方程式为_________________;为使生成的Cl2完全被吸收,则电源的a极应为___极(填“正”或“负”),溶液中生成NaClO的离子方程式为____________________。
甲醇是一种可再生能源,具有广泛的开发和应用前景。
(1)已知:CO(g)+1/2O2(g)=CO2(g) △H=—283 kJ·mol—1
2H2(g)+O2(g)=2H2O(l) △H=—285.8 kJ·mol—1
CH3OH(l)+3/2O2(g)=CO2(g) +2H2O(l) △H=—725kJ·mol—1
则反应CO(g)+2H2(g)=CH3OH(l)的△H=_______。
(2)工业上合成甲醇一般采用下列反应:CO(g)+2H2(g) CH3OH(g) △H="—a" kJ/mol(a>0),H2的平衡转化率与温度、压强的关系如下图所示。
CH3OH(g) △H="—a" kJ/mol(a>0),H2的平衡转化率与温度、压强的关系如下图所示。
压强:P1 P2(填“>”、“=”或“<”)。
(3)在容积固定的密闭容器中发生CO(g)+2H2(g) CH3OH(g) △H="—a" kJ/mol(a>0),各物质的浓度如下表:
CH3OH(g) △H="—a" kJ/mol(a>0),各物质的浓度如下表:
| 浓度mol/L 时间/min |
c(CO) |
c(H2) |
c(CH3OH) |
| 0 |
0.8 |
1.6 |
0 |
| 2 |
0.6 |
1.2 |
0.2 |
| 4 |
0.3 |
0.6 |
0.5 |
| 6 |
0.3 |
0.6 |
0.5 |
①反应从2 min到4 min之间,H2的反应速率为 。
②反应达到平衡时CO的转化率为 。
③反应在第2 min时改变了反应条件,改变的条件可能是 (填序号)。
A.使用催化剂B.降低温度C.增加H2的浓度
(4)甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,实验室用如图装置模拟该过程,其原理是:通电后,Co2+被氧化成Co3+,然后以Co3+做氧化剂把甲醇氧化成CO2而除去(Co3+的还原产物是CO2+)。
①写出阳极电极反应式_____________________________________;
②写出除去甲醇的离子方程式_______________________________。
【化学——有机化学基础】(共15分)
(1)今有如下图所示的三种有机物:
①写出丙中含氧官能团的名称 ;
②这三种物质中,互为同分异构体的是 ;
③写出乙和过量NaOH溶液共热时反应的化学方程 。
(2)由丙烯经下列反应可制得F、G两种高分子化合物,它们都是常用的塑料。
①A的同分异构体还有 种;
②聚合物F的结构简式是 ;
③B转化为C的化学方程式是 ;
写出与E具有相同官能团的一种同分异构体的结构简式 ;
I.甲、乙、丙、丁四种物质存在转化关系:
(1)若甲、乙均为空气主要成分,则丁与水反应的化学方程式为 。
(2)若甲为常见的固体非金属单质,丙可使品红溶液褪色,则丁为____________。
(3)若乙是生活常见金属单质,丙→丁的离子方程式为 。
(4)若丙既能与强酸又能与强碱反应,则丙的化学式为 (任写1种)。
II.一定温度下,容积为1 L的密闭容器中投入0.5 mol PCl5(g),存在平衡:PCl5(g) PCl3(g)+ Cl2(g)。反应过程中测得部分数据如下表:
PCl3(g)+ Cl2(g)。反应过程中测得部分数据如下表:
| 时间 |
n(PCl5)/mol |
n(PCl3)/mol |
n(Cl2)/mol |
| 0 |
0.5 |
0 |
0 |
| t1 |
0.45 |
||
| t2 |
0.1 |
||
| t3 |
0.4 |
(5)t1时刻,测得反应吸收的热量为a kJ。PCl3(g)与Cl2(g)反应的热化学反应方程式为 。
(6)t2时:v正 v逆(填“>”、“<”或“=”)。
(7)计算该反应的化学平衡常数K=_____________。相同温度下,改为往容器中投入0.2 mol PCl5(g)、0.2 mol PCl3(g)、0.1 mol Cl2(g),到达平衡前,PCl5的物质的量将 (填“增大”、“减小”、“不变”)。
选做[化学一选修5:有机化学基础)芳香族化合物水杨酸、冬青油、阿司匹林都是常用西药。它们的结构简式如下表:
(1)水杨酸分子中式量较大的含氧官能团名称是 。
(2)水杨酸在浓硫酸催化作用下与乙酸酐(CH3C0)20反应生成阿司匹林,反应的化学方程 。
(3)水杨酸在一定条件下可以聚合成高分子化合物聚水杨酸,聚水杨酸的结构简式为: 。
(4)写出冬青油的一种同分异构体结构简式:_____________________
异构体符合以下条件:
①芳香族化合物;
②苯环上一个氢原子被氯取代,有两种可能的产物;
③在足量氢氧化钠溶液中充分反应消耗等物质的量氢氧化钠。
(5)阿司匹林晶体中残留少量的水杨酸,可用 _____________(填试剂名称)检验.
实验室利用阿司匹林和水杨酸在乙酸乙酯中溶解度的差异,用结晶法提纯阿司匹林,请完成以下实验操作步骤:
①用少量热的乙酸乙酯溶解晶体.②________③经__________操作得到纯净的阿司匹林晶体。
(6)效更佳的长效缓释阿司匹林( )在人体内可缓慢释放出阿司匹林分子,反应的化学方程式为 ,反应类型为 。
)在人体内可缓慢释放出阿司匹林分子,反应的化学方程式为 ,反应类型为 。