Ⅰ.中学课本中介绍了如下实验:把一端弯成螺旋状的铜丝放在酒精灯外焰加热,待铜丝表面变黑后立即把它插入盛有约2 mL乙醇的试管里,反复操作几次。
请你评价若用上述方法制取乙醛存在哪些不足(写出一点即可)。
Ⅱ.某课外活动小组利用下图装置进行乙醇的催化氧化实验并制取乙醛,图中铁架台等装置已略去,粗黑线表示乳胶管。请填写下列空白: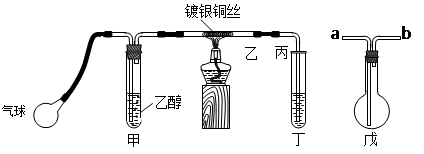
(1)甲装置常常浸在70~80℃的水浴中,目的是 。
(2)若试管丁中用水吸收产物,则要在导管乙、丙之间接上戊装置,其连接方法是(填戊装置中导管代号):乙接 、_______接丙;若产物不用水吸收而是直接冷却,应将试管丁浸在 _____ 中。
利用生活中或实验室中常用的物品(电极材料、导线、电解质溶液、电流计),根据实验原理:Zn+2H+==Zn2++H2↑,根据选取材料自己动手设计一个原电池。
(1)选取的负极材料为,电解液为:
(2)电子由极经外电路流向极(填“正和负”)
(3)负极的电极反应式:。
(4)正极发生(“氧化”或“还原”)反应,周围会出现的现象是。
下表为元素周期表的一部分,列出10种元素在周期表中的位置。用化学符号回答下列问题:
(1)10种元素中,化学性质最活泼的金属是。
(2)④、⑤、⑥三种元素最高价氧化物对应的水化物中,碱性最强的是。
(3)③、④三种元素形成的离子,离子半径由大到小的顺序是。
(4)④和⑨两种元素形成化合物的化学式为,该化合物燃烧时的焰色为,该化合物溶液与元素⑧的单质反应的离子方程式为。
短周期元素X、Y、Z、W核电荷数依次增大,X、Z同主族,Z、W同周期,四种元素的原子序数之和为37,在周期表中X是原子半径最小的元素,Y的最外层电子数是内层电子数的3倍。
(1)W在周期表中的位置是第周期第族。
(2)X与Y 能形成具有18个电子的化合物,此化合物的电子式为。
(3)X、Y、Z三种元素组成的化合物中存在(填“化学键”名称)。
(4)Y、Z、W形成的某种化合物晶体类型是(填“晶体类型”名称)。
(5)X和Y形成的化合物沸点比X和W形成的化合物沸点(填“高”或“低”)。
(6)Z、W两种元素的最高价氧化物对应水化物溶液之间反应的离子方程式为。
现有①BaCl2②金刚石③碘片 ④冰 ⑤Na2SO4五种物质,按下列要求回答(填编号)
(1)熔化时不需要破坏化学键的是,熔化时需要破坏共价键的是;
(2)只有离子键的物质是,含有共价键的离子化合物是。
有下列各组物质
| A.O2和O3 |
| B.12C和13C |
C.CH3—CH2—CH2—CH3和 |
| D.H2O和D2O |
E.液氯和氯气
F.CO(NH2)2和NH4CNO
G.C60和金刚石
(1)组两物质互为同位素;
(2)组两物质互为同素异形体;
(3)组两物质互为同分异构体;
(4)组中两物质是同一物质。