氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质。为了提纯氯化钾,先将样品溶于适量水中,充分搅拌后过滤,再将滤液按如下图所示步骤进行操作(注意事项:①所加试剂必须过量;②过量试剂必须除去;③不能引入新的杂质)。
回答下列问题:
(1)试剂Ⅰ的化学式为 ,①中发生反应的离子方程式为
。
(2)试剂Ⅱ的化学式为 ,②中加入试剂Ⅱ的目的是 。
(3)试剂Ⅲ的名称是 ,③中发生反应的离子方程式为 。
(4)某同学称取提纯的产品0.775 9 g,溶解后定容在100 mL容量瓶中,每次取25.00 mL溶液,用硝酸银溶液反应共消耗硝酸银0.002 562 mol,则该产品的纯度为
。
短周期主族元素A、B、C、D、E在元素周期表中的位置如图所示: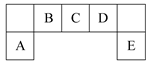
(1)B、C、D元素电负性的大小顺序为:>>(填元素符号)。
(2)E的氢化物与其最高价氧化物对应的水化物的钾盐共热能发生反应生成一种气体单质,反应的化学方程式为。
(3)C有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2 L甲气体与0.5 L氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的含氧酸盐的化学式是。
(4)在298 K下,A、B的单质各1 mol完全燃烧,分别放出热量a kJ和b kJ。又知一定条件下,A的单质能将B从它的最高价氧化物中置换出来,若此置换反应生成3 mol B的单质,则该反应在298 K下的ΔH=。(注:题中所设单质均为最稳定单质)
(5)要证明与D同主族相邻元素F的非金属性与E的非金属性的强弱,正确、合理的实验操作及现象是。
(6)用A、B的单质作电极,C的最高价氧化物对应水化物的浓溶液作电解质溶液构成原电池,写出此原电池正极的电极反应式。(假设C只被还原至+4价)
现有部分短周期元素的性质或原子结构如下表:
| 元素编号 |
元素的性质或原子结构 |
| X |
最外层电子数是次外层电子数的3倍 |
| Y |
常温下单质是双原子分子,其氢化物的水溶液显碱性 |
| Z |
第三周期元素的简单离子中半径最小 |
(1)元素X的一种单质在生活中常用作饮水机的消毒剂,该单质的化学式是,元素Z的离子结构示意图为。
(2)元素Y与氢元素形成一种离子YH4+,请写出检验溶液中存在该离子的实验操作、现象和结论。
(3)写出Z元素最高价氧化物对应的水化物与NaOH溶液反应的离子方程式:。
(4)元素X与元素Y相比,非金属性较强的是(用元素符号表示),下列表述中能证明这一事实的是。
a.Y的氢化物可在纯X2中燃烧生成X的氢化物和Y2
b.X的单质比Y的单质更容易与H2化合
c.X与Y形成的化合物中Y元素呈正价态
六种短周期元素,aA、bB、cC、dD、eE、fF,已知原子序数大小关系是:a<e<c<b<f<d,且a+b=(c+d)/2;六种元素在周期表中的位置关系是:A、B同主族,C、D也同主族;C、E相邻,B、F也相邻。
(1)B、C、D三种元素形成的六原子核的化合物和水反应的离子方程式是:。
(2)A、C形成的四原子核化合物甲的电子式为,该化合物呈弱酸性,试写出这种化合物的电离方程式:。
(3)写出分别由A、B、C、D四种元素所形成的两种化合物的水溶液相互反应的离子方程式:。
(4)写出A、C、D形成的六原子核化合物乙的水溶液和甲的水溶液反应的化学方程式:。
(5)写出E和F形成的化合物和化合物A2C反应的化学方程式:。
(6)A、E形成的四原子核化合物丙容易液化,其原因是:。
下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题: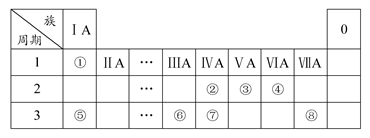
(1)④⑤⑥的原子半径由小到大的顺序为(用元素符号表示);
②③⑦的最高价含氧酸的酸性由弱到强的顺序是(用化学式表示)。
(2)写出由以上某些元素构成的既含离子键、又含极性共价键的化合物的电子式(写出一种即可)。
(3)已知常温下1 g①单质在④单质中燃烧生成稳定的液态物质时放出142.9 kJ热量,则表示①单质燃烧的热化学方程式为。
(4)①②形成的最简单的化合物与④单质在KOH作电解质溶液时可形成原电池,其中负极的电极反应为。
(5)由表中元素①③④⑥⑧所形成的常见物质X、Y、Z、M、N可发生以下反应: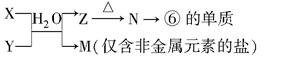
①X溶液与Y溶液反应的离子方程式为;
②N→⑥的单质所采用的方法是;
③M溶液呈酸性,原因是(用离子方程式解释)。
硫、氮、碳、铁、铜等常见元素在化合物中常表现出多种价态,如硫有-2、-1、+2、+4、+6等价态。这些元素在化工生产中有着重要应用。
(1)31.2g镁与碳粉的混合物在一定条件下恰好完全反应,再加入足量水,得到40.6g白色沉淀,同时产生密度为1.4107g/L(标准状况)的丙二烯和不饱和烃X的混合气体。
①镁与碳粉的反应产物的化学式为 ______________ 。
②原混合物中碳粉的物质的量分数为 ___________。(用小数表示,保留2位小数)
(2)某复杂盐由三种元素组成,含两种阳离子和两种阴离子。取21.76g该复杂盐,平均分为两份。将第一份溶于足量盐酸酸化的氯化钡溶液,所得沉淀中含9.32g硫酸钡。将第二份溶于足量热浓硝酸,再滴加足量硝酸钡溶液,得13.98g白色沉淀,过滤后向蓝色滤液中加足量烧碱溶液,过滤、洗涤、灼烧,得8.00g黑色固体。
①该复杂盐的化学式为_____________。
②该复杂盐中两种阳离子的质量比为 _________________ 。
(3)某地质学家经勘测发现一种新的磁黄铁矿,主要成分为Fe1-xS1+x,杂质不含Fe、S。分析可知该磁黄铁矿中,铁元素中三价铁的质量分数为75%。取5吨 73%的该磁黄铁矿,用接触法制硫酸,若沸腾炉中煅烧的损耗率为4%,接触室中反应的转化率为94%,SO3的吸收效率为97%,则最多可制得98.3%的浓硫酸的质量是________________。(保留2位小数)